قبل خمسة وسبعين عامًا، ثبت أن الأوعية الدموية الشريانية والوريدية الكبيرة في السحايا حساسة للألم، على عكس نسيج الدماغ نفسه. قبل خمسة وعشرين عامًا، تم تحديد الببتيدات العصبية، أي البروتينات التي تفرزها الألياف العصبية، والتي تنظم قطر هذه الأوعية الدموية. إحدى هذه المواد هي CGRP ( الببتيد المرتبط بجين الكالسيتونين ). يُعد CGRP من أقوى موسعات الأوعية الدموية في الجسم. في الوقت نفسه، يترافق توسع الأوعية الدموية الناتج عن CGRP مع الألم في التجارب.
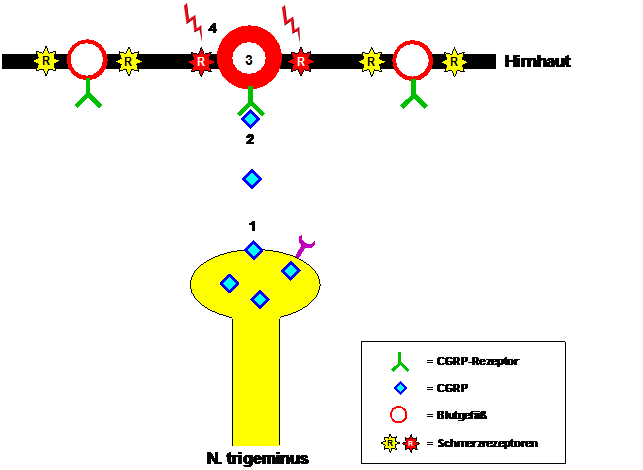
برز الدور المحوري لـ CGRP في تطور الصداع النصفي عندما وُجدت مستويات مرتفعة منه في الدم الوريدي لمرضى يعانون من نوبات الصداع النصفي. وقد عادت هذه المستويات إلى طبيعتها بعد انحسار الصداع النصفي عقب تناول دواء سوماتريبتان. وتأكدت هذه الملاحظات عندما أمكن تحفيز نوبات الصداع النصفي لدى المرضى عن طريق حقن CGRP. يُنتَج CGRP، من بين أماكن أخرى، في الألياف العصبية للعصب ثلاثي التوائم، ويُفرَز عند تنشيطها أثناء نوبة الصداع النصفي (انظر الشكل 1). يرتبط CGRP المُفرَز بمستقبلات CGRP في جدران الأوعية الدموية في السحايا، مما يؤدي إلى توسع الأوعية الدموية، وفي الوقت نفسه إلى تحسس مستقبلات الألم في جدران الأوعية الدموية. يصبح نبض الأوعية الدموية المتوسعة هو محفز الألم، الذي يشعر به المرضى على شكل ألم نابض وشديد في الصداع النصفي، يزداد مع أي مجهود بدني، حتى عند الانحناء.
الشكل 1: توسط CGRP في ألم الصداع النصفي. أثناء نوبة الصداع النصفي، يتم إطلاق CGRP (1) من ألياف العصب ثلاثي التوائم، ويرتبط بمستقبل CGRP (2)، ويحفز توسع الأوعية الدموية في السحايا (3) ويؤدي في النهاية إلى تحسس مستقبلات الألم (4) التي تستجيب لنبض الأوعية الدموية المجاورة بإحساس ألم الصداع النصفي النابض.
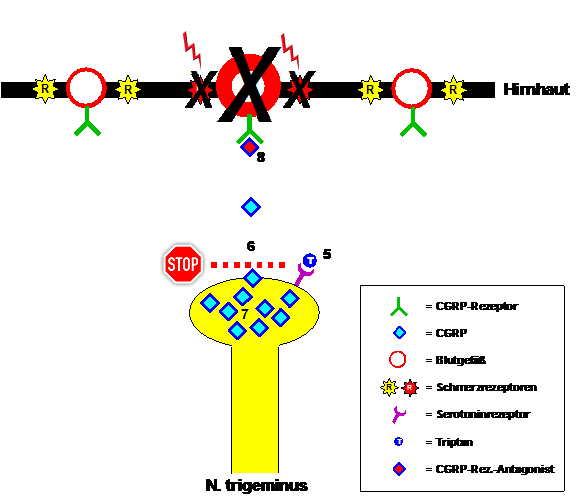
ترتبط التريبتانات بمستقبلات السيروتونين المحددة الموجودة في نهايات ألياف العصب ثلاثي التوائم، وتثبط إطلاق الببتيد المرتبط بجين الكالسيتونين (CGRP) أثناء نوبة الصداع النصفي. يستغرق الأمر بعض الوقت حتى يتحلل CGRP الذي تم إطلاقه سابقًا، وحتى تنقبض الأوعية الدموية مرة أخرى، وحتى تستعيد مستقبلات الألم حساسيتها الطبيعية. عندها، يتوقف الصداع النصفي مؤقتًا لدى المريض. وهذا يوضح أن التريبتانات، كأي دواء آخر، تعمل بشكل أسرع وأكثر فعالية كلما تم تناولها مبكرًا أثناء النوبة، وكلما قلّ إطلاق CGRP. مع ذلك، يتضح أيضًا أن التريبتانات لا تنهي نوبات الصداع النصفي. يستمر إنتاج CGRP، ولكن يتم تثبيط إطلاقه مؤقتًا. يتراكم CGRP في ألياف العصب ثلاثي التوائم، في انتظار استقلاب التريبتانات. يؤدي الإطلاق اللاحق، وأحيانًا بكميات كبيرة، لـ CGRP إلى عودة ألم الصداع النصفي لدى المرضى، وهو ما يُعرف بالصداع الارتدادي. عادةً ما يكون تناول جرعة أخرى من التريبتان فعالًا مرة أخرى. تتكرر هذه الدورة حتى تهدأ نوبة الصداع النصفي نهائيًا، عادةً بعد 4 إلى 72 ساعة. وكبديل للتريبتانات، جُرِّبت أدوية قبل عدة سنوات لا تمنع إطلاق الببتيد المرتبط بجين الكالسيتونين (CGRP)، بل تمنع مستقبلات CGRP نفسها. وبالتالي، لم يجد CGRP المُطلق أي هدف في نوبات الصداع النصفي. كانت مضادات مستقبلات CGRP هذه فعالة بشكل مشابه للتريبتانات، ولكن لسوء الحظ، أدى الاستخدام المنتظم بجرعات عالية إلى تلف الكبد، لذا لم تُطرح في الأسواق.
الشكل 2: علاج نوبة الصداع النصفي باستخدام التريبتانات ومضادات مستقبلات CGRP. ترتبط التريبتانات بمستقبلات السيروتونين على نهايات العصب ثلاثي التوائم (5)، وبالتالي تثبط إطلاق CGRP (6). فتخف أعراض الصداع النصفي الناتجة عن CGRP. ويمكن تحقيق التأثير نفسه عن طريق حجب مستقبلات CGRP باستخدام مضادات مستقبلات CGRP (8). تكمن مشكلة التريبتانات في أنه حتى بعد زوال الصداع النصفي ظاهريًا، يستمر إنتاج CGRP (7) ثم يُطلق بعد زوال تأثير التريبتان، مما يؤدي إلى تكرار الصداع.
كان إدخال التريبتانات بلا شكّ تقدماً حاسماً في نوبات . وحتى الآن، لم يتحقق نجاح مماثل في الوقاية الصداع النصفي تُطوّر . جميع هذه الأدوية استُخدمت في البداية لعلاج حالات أخرى، مثل حاصرات بيتا لعلاج ارتفاع ضغط الدم، ولها نسبة فائدة إلى مخاطر غير مواتية إلى حدٍّ ما. من المتوقع أن يتغير هذا الوضع في المستقبل، ومرة أخرى، يلعب الببتيد المرتبط بجين الكالسيتونين (CGRP) دوراً حاسماً.
تُجرى حاليًا تجارب سريرية، بمشاركة عيادة كيل للألم، الأجسام المضادة وحيدة النسيلة للوقاية من الصداع النصفي. تعمل هذه الأجسام المضادة إما على تدمير بروتين CGRP، الذي يُفرز أثناء نوبات الصداع النصفي، أو تستهدف مستقبلات CGRP. وبذلك، يُحصّن المرضى بشكل غير مباشر ضد الصداع النصفي. تُعطى الأجسام المضادة تحت الجلد مرة واحدة شهريًا. تُشير نتائج الدراسة الأولية إلى نتائج واعدة، حيث أثبتت هذه المواد فعاليتها بشكل ملحوظ مقارنةً بالدواء الوهمي، كما أنها لاقت استحسانًا جيدًا حتى الآن. لكن ما يُشجع على وجه الخصوص للمستقبل هو أن مجموعة صغيرة من المرضى في تجارب المرحلة الثانية المنشورة قد شفوا تمامًا من نوبات الصداع النصفي. يبقى أن نرى ما إذا كانت هذه النتائج ستُؤكد، والأهم من ذلك، ما إذا كانت هذه التأثيرات ستستمر.
الشكل 3: هدف الأجسام المضادة وحيدة النسيلة للوقاية من الصداع النصفي. تُحقن هذه الأجسام المضادة تحت الجلد مرة واحدة شهريًا، ثم تعمل إما على تدمير الببتيد المرتبط بجين الكالسيتونين (CGRP) (9) الذي يُفرز أثناء نوبات الصداع النصفي، أو على تدمير مستقبلات CGRP (10). نظريًا، من المفترض أن يمنع هذا تحول نوبات الصداع النصفي إلى نوبات غير مؤلمة نتيجةً لإلغاء تأثير CGRP.
الدكتور أكسل هاينز، الدكتورة كاتيا هاينز كون، البروفيسور الدكتور هارتموت جوبل، عيادة كييل للألم
إضافة: استفسر العديد من القراء عن المشاركة في الدراسة. للمشروع معايير محددة للمشاركة، والتي يجب مراجعتها بشكل فردي. إنها دراسة دولية. ولضمان إمكانية مقارنة النتائج على مستوى العالم، لا يمكن لكل مركز اختيار سوى عدد محدود من المشاركين. وهذا يتطلب عادةً فترات علاج أطول في عياداتنا الخارجية.










أوافقك الرأي، فأنا أيضاً أعاني من الصداع النصفي منذ سنوات طويلة، وهو لا يزول أبداً. أحياناً لا يُجدي أي شيء نفعاً، حتى أنني أضطر للاتصال بخدمات الطوارئ. أتمنى حقاً أن أحصل على التطعيم، على أمل أن يزول هذا الصداع نهائياً.
أعاني من الصداع النصفي منذ أن كنت في الثامنة عشرة من عمري. الآن عمري 59 عامًا، وقد جربتُ الكثير من الحلول، لكن دون جدوى. كل هذه المحاولات الفاشلة أصابتني بالإحباط. حاليًا، أخضع لعلاج البوتوكس، وقد خفّض هذا العلاج عدد أيام الألم من 15 إلى 20 يومًا شهريًا إلى 12 إلى 15 يومًا في المتوسط. هذا تحسن طفيف. لكن الوضع يزداد سوءًا عندما ينفد مخزوني من 10 أقراص تريبتان شهريًا، فأضطر لتحمل الألم لبقية الشهر. أحيانًا أشعر وكأنني أكافح من أجل البقاء.
سيكون لقاح الصداع النصفي - الذي ذكره طبيب الأعصاب أيضًا - رائعًا، وسيمنح الكثيرين فرصة لتحسين جودة حياتهم.
إذا أُجريت دراسات إضافية في ألمانيا، واحتجنا إلى مشاركين، فسأكون سعيدًا جدًا بالمشاركة.
أعاني أنا أيضاً من الصداع النصفي منذ أكثر من ثلاثين عاماً. أحياناً مصحوباً بهالة، لكن في أغلب الأحيان بدونها. إنه ألم مبرح يدفعك إلى الاكتئاب. لا يمكنك التخطيط لأي شيء بشكل صحيح، ويصعب عليك الاستمرار في العمل. تأتي النوبات بشكل غير متوقع. لا يمكنك التعامل مع ضغوط الحياة اليومية بسببها. لا تجد تفهماً إلا لدى من يفهمونك. أنا أيضاً سأتطوع لتلقي اللقاح حتى تصبح الحياة جديرة بالعيش من جديد.
سأتطوع أيضًا للمشاركة في هذه الدراسة!
منذ أن غيرت طبيبي، أصبحت أعاني من نوبات متكررة، وتم تشخيصي بالدوار والصداع النصفي. حتى يوم واحد أقل بدون صداع نصفي هو يوم مكسب. وأتمنى بشدة أن تتحقق أمنيتي الكبرى.
أعاني أيضاً من الصداع النصفي منذ أربعين عاماً، وتزداد وتيرته عاماً بعد عام، ليصل إلى حوالي عشرين مرة شهرياً. لا يسعك إلا أن تستسلم للألم عاجزاً، ويعاني معك أهلك وأصدقاؤك وزملاؤك.
عندما رأيت التقرير على موقع Visite، كدتُ أبكي أملاً في مستقبل خالٍ من الألم. ومثل كثيرين هنا، كنتُ
سأسجل فوراً كمتطوع في التجربة.
هل ما زالت المعجزات ممكنة؟
سأشارك في الدراسة فوراً... أعاني من الألم لمدة 30 يوماً في الشهر -.-
أودّ بشدة المشاركة في هذه الدراسة.
أعاني من الصداع النصفي منذ طفولتي، وقد باءت جميع العلاجات التي جربتها بالفشل. أعاني من نوبات صداع نصفي حادة للغاية، حتى أن الأدوية لم تعد تُجدي نفعًا. غالبًا ما أبقى طريح الفراش أشعر بالخمول، ويعاني جميع أفراد عائلتي من ذلك. لعلّ هذا العلاج يكون بمثابة راحة لي ولعائلتي!
مع أطيب التحيات من فرانكفورت!
أنا أغبطكِ على تعليقاتكِ! o.0 تم تشخيص إصابتي بالصداع النصفي عندما كنت في الخامسة أو السادسة من عمري، وأعاني منه لمدة تصل إلى 25 يومًا في الشهر... أتطلع بشوق إلى الدواء، وسأفعل أي شيء لأشعر ببعض الراحة... أنا أؤجل عملية استئصال القوقعة فقط بسبب الدواء... لكن خمس مرات في الشهر تُعد نتيجة جيدة تقريبًا! oO
أعاني من الصداع النصفي منذ 38 عامًا. عشتُ معه مدةً أطول من المدة التي عشتها بدونه. لا أستطيع حتى حصر كل ما جربته، وتشبثتُ بكل أملٍ ممكن. كل ذلك دون جدوى. أكره كيف يُسيطر الصداع النصفي على حياتي/حياتنا. في النهاية، أضطر دائمًا إلى اللجوء إلى التريبتانات لأتمكن من الذهاب إلى العمل والمشاركة في الحياة ولو بشكلٍ ما. لا أصدق أن اللقاح سيكون أعظم هدية لي بعد كل هذا الوقت.
أؤيد ما قاله من سبقونا. بعد عقود من الألم وتجارب علاجية لا حصر لها، سيكون هذا العلاج/اللقاح بمثابة خلاص. جميعنا نتوق إليه، وجميعنا بحاجة إلى علاج يُعيد إلينا جودة حياتنا. نكافح يومًا بعد يوم وأسبوعًا بعد أسبوع، وكل دقيقة من حياتنا تُخيم عليها نوبات الصداع النصفي. عقولنا وأرواحنا وأجسادنا تتألم. كل واحد منا يستحق التقدير على الإنجازات التي نحققها رغم الألم. وهذا يشمل الباحثين الذين يُجرون أبحاثًا حول الصداع النصفي نيابةً عنا. شكرًا لكم.
كنتُ سأكون هناك أيضاً – منذ أن كان عمري 14 عاماً – وكما قلتُ – لا أحد يُصدّق مدى تأثير ذلك على الحياة اليومية.
ليس المريض وحده من يُعاني – بل الأطفال، والشركاء، والزملاء – لا أحد يُراعي ذلك.
سأدفع ثمن التطعيم فوراً، لأنني أعاني من الصداع النصفي المصحوب بهالة منذ 35 عاماً، ومنذ انقطاع الطمث قبل حوالي عام، أصبحت أعاني من نوبات أكثر تكراراً كل شهر مما كنت عليه من قبل.
سأنضم فوراً. من الصعب تخيل التخلص من الصداع النصفي مجدداً بعد سنوات من المعاناة منه. مجرد عيش الحياة والاستمتاع باليوم.
أكثر من 350 يومًا في السنة بدون ألم؟ هذا يبدو رائعًا لدرجة يصعب تصديقها!
سيكون ذلك بمثابة حلم يتحقق!!! بعد ما يقرب من 30 عامًا ومعاناة من 4-5 نوبات صداع نصفي شهريًا، أخيرًا بدون ألم!!! سأكون مستعدًا للمشاركة في الدراسة فورًا.
بلا ألم، يا لها من كلمة جميلة..
أعاني من الصداع النصفي الحاد منذ أن كان عمري 17 عامًا. الآن عمري 56 عامًا، وقد عانيت من الصداع النصفي لثلاثة أيام متتالية. كل ثلاثة أشهر، أتلقى 18 قرصًا من دواء ماكسالت للصداع النصفي وأربع حقن من دواء إيميجران، مما يجعل حياتي اليومية أكثر احتمالًا. سأكون سعيدًا جدًا لو تخلصت أخيرًا من نوبات الصداع التي لا تُطاق من خلال التطوع كمتطوع في تجربة سريرية.
أن أكون أخيرًا خاليًا من الألم وأن أعود ببساطة إلى ممارسة حياتي الطبيعية - سيكون ذلك حلمي.
أيها الأطباء الأعزاء،
إن فكرة احتمال انخفاض الألم بعد حوالي 60 عامًا تبدو مثالية. ومثل كثيرين غيري، سأتطوع فورًا للمشاركة في التجربة. لعلها تنجح يومًا ما. مع
أطيب التمنيات لنا جميعًا،
غونار ثيم.
يبدو الأمر أشبه بقصة خيالية، سيكون ثوريًا حقًا - جرعة واحدة شهريًا وسيكون كل شيء على ما يرام... سأتلقى التطعيم أسبوعيًا أيضًا، والأهم هو التخلص من الخوف من نوبة الصداع النصفي!
أن أستمتع بالحياة مجددًا، دون الشعور بالذنب تجاه زملائي، وهكذا دواليك... أتمنى أن أكون هناك!
سأتطوع فورًا للمشاركة! أعاني من الصداع النصفي منذ زمن طويل، ويبدو أنني أصبحت أكثر حساسية له، أو بالأحرى، أصبح الصداع النصفي أكثر تكرارًا، دون سبب واضح! جربتُ جميع أنواع الأدوية الوقائية للصداع النصفي، وتوقفتُ عن تناولها جميعًا لأنها لم تُجدِ نفعًا. إذن، كيف يُمكنني المشاركة في الدراسة؟ تبدأ التعليقات في مارس 2015، أليس كذلك؟ اليوم، عندما صادفتُ هذه الصفحة لأنني أعاني من نوبة صداع نصفي أخرى، كان التاريخ هو 19 سبتمبر 2016!
أنا موافق فوراً! حياة بلا ألم تبدو مثالية لدرجة يصعب تصديقها..
أنا مهتم جدًا أيضًا بالمشاركة كشخص خاضع للتجربة والهروب من هذه الحلقة المفرغة
عزيزي البروفيسور الدكتور هارتموت جوبل، أعزائي الدكاترة. أكسل هاينز وكاتيا هاينز-كون،
أشارككم الآمال الكثيرة التي عبّر عنها المعلقون. هل لي أن أقترح اقتراحًا بخصوص ملاحظاتكم القيّمة والمفيدة؟ يذكر المقال، من بين أمور أخرى، نتائج دراسات المرحلة الثانية المنشورة. أودّ الاطلاع على الجدول الزمني المقترح للتخطيط للمرحلة التالية (المرحلة الثالثة، تاريخ إنجاز الملف التنظيمي، وتاريخ الموافقة المتوقع).
بحسب تجربتي، يلعب الأمل دورًا هامًا في علاج الصداع النصفي. على سبيل المثال، حتى المجموعة التي تلقت حقنة وهمية فقط أظهرت تحسنًا. أبلغ من العمر 59 عامًا وأتناول ما بين 8 إلى 10 أقراص من التريبتانات شهريًا. وبما أن هذه الأدوية أقل شيوعًا بعد سن 65، فأنا أفكر بالفعل فيما سيحدث خلال السنوات القليلة القادمة. حاليًا، لا يوجد بديل حقيقي للتريبتانات بالنسبة لي، مما يجعل فكرة عدم القدرة على تناولها بعد بضع سنوات أمرًا مزعجًا. لذلك، فإن التخطيط للمستقبل يهمني كثيرًا (وأعتقد أنني أتحدث باسم العديد من المعلقين هنا). من يدري، ربما مجرد احتمال الحصول على المساعدة - حتى لو كانت بعيدة - سيحسن الوضع اليوم. لا أستطيع استبعاد هذا الاحتمال بالنسبة لي. ففي النهاية، "الأمل لا ينقطع".
مع أطيب التحيات وأتمنى لكم كل التوفيق!
شاهدتُ أمس برنامج "زيارة" على قناة NDR، ورأيتُ أن هناك لقاحًا للصداع النصفي. سأحصل على اللقاح فورًا. منذ انقطاع الطمث، الذي كان صعبًا للغاية، أعاني من الصداع النصفي بشكل شبه يومي. أحيانًا يكون خفيفًا، وأحيانًا يكون حادًا، لكنه دائمًا موجود. قوتي تتلاشى تدريجيًا، ونوعية حياتي متدنية للغاية لدرجة أنني أحيانًا لا أرغب في الاستمرار. عمري 56 عامًا، وأتساءل كيف ستستمر الأمور. لو كان هناك دواء كهذا، لكان الأمر رائعًا حقًا. من المؤسف أننا، كمواطنين عاديين، نكتشف هذه الأمور دائمًا بعد فوات الأوان. سيكون حلمًا أن أتخلص من الألم والضعف مجددًا. سأصبح جدة للمرة الأولى، ويحزنني جدًا أنني لن أكون بصحة جيدة بما يكفي لذلك
عزيزي الأستاذ غوبل،
أتمنى لك وللأطباء المشاركين الآخرين كل التوفيق. ستكون هذه ثورة في علاج الصداع النصفي. أنا أتطلع إليها بشوق.
مع أطيب التحيات،
س. ريتر
من المذهل عدد الأشخاص الذين يعانون من نفس المشكلة، ومع ذلك نادرًا ما تصادف أشخاصًا يشاركونك نفس التفكير في حياتك اليومية! بعد ثلاثين عامًا من المعاناة مع الصداع النصفي وتجربة جميع أنواع العلاجات والأدوية التي لم تُجدِ نفعًا، تمنحني هذه الدراسة أملًا كبيرًا! لديّ طفل صغير منذ تسعة أشهر، وكما تتخيلون، فإنّ وجود طفل مع الصداع النصفي هو أسوأ مزيج يمكن تخيله. أتمنى بشدة أن يأتي يوم لا أخشى فيه نوبات الصداع النصفي بعد الآن، وأن أستمتع بالحياة كما يستمتع بها من لا يعانون من الألم!
أعاني من الصداع النصفي منذ سنوات، ولا أتحمل الأقراص جيدًا. تعاني ابنتاي أيضًا من الصداع النصفي. أخشى دائمًا تناول القرص لأنه يسبب لي الغثيان وانخفاض ضغط الدم. أود بشدة المشاركة كمتطوعة في التجربة.
تلقيت العلاج في عيادة كيل للألم في سبتمبر 2015. أعاني من الصداع النصفي المزمن! التعايش مع هذا الأمر صعب للغاية، سواء في العمل أو في حياتي الشخصية! سأفعل أي شيء لأتمتع بصحة جيدة! سأشارك كمتطوعة في التجارب فورًا...
حياة بلا ألم - يا لها من روعة!
أليس ذلك رائعاً؟ أن نتمتع بعقل "طبيعي"، وأن ننام نوماً هانئاً، وأن نعيش كل يوم... كل يوم!
ترقبوا المزيد!
أعاني من الصداع النصفي منذ حوالي ٢٦ عامًا، وسأكون سعيدًا بالتطوع كمتطوع لتجربة هذا الأمر! حياة بلا صداع نصفي!!! أمر لا يُصدق، رائع، مذهل...
سأنضم فوراً! نصف أسبوع من الألم المبرح، 52 أسبوعاً في السنة – لا أحد يستطيع تحمل ذلك! أخيراً تحررت!
أعاني من الصداع النصفي منذ طفولتي، مصحوبًا بالغثيان والقيء في كل مرة؛ إنه كابوس، ويستمر معي منذ ما يقارب الثلاثين عامًا. أتناول دواء سيتالوبرام لنوبات الهلع منذ بضع سنوات. أخشى تجربة التريبتانات بسبب التفاعلات الدوائية المحتملة. الأدوية الأخرى لا تُجدي نفعًا معي. هذا يعني أنني أستطيع التعايش مع الصداع بدون دواء في كل مرة. تُصيبني نوبة الصداع مرة أو مرتين شهريًا، فأضطر بعدها إلى الاستلقاء في الفراش والتقيؤ. لذا، فإن حياةً خالية من الصداع النصفي ستكون حلمًا، بل أمنيتي الكبرى.
سيكون ذلك نعمة!
أعاني من الصداع النصفي منذ خمسين عامًا، وقبل عشر سنوات أصبت بالاكتئاب أيضًا. سأتطوع فورًا للمشاركة في التجارب السريرية لاستعادة جودة حياتي الطبيعية. سيكون هذا الاختراع نعمة!
بعد حوالي ٢٨ عامًا من المعاناة مع الصداع النصفي وتجربة جميع الأدوية الوقائية، أتمنى بشدة الحصول على لقاح شهري والتخلص من الصداع النصفي نهائيًا. آمل أن يصبح هذا الأسلوب متاحًا للجميع قريبًا.
تم تشخيص إصابتي بالصداع النصفي المزمن.
سأكون سعيداً بالمشاركة في دراسة على الفور.
يا للعجب، كل هذه التعليقات، وكأنني أنا من كتبتها. عمري 42 عامًا وأعاني من الصداع النصفي منذ نعومة أظفاري. أتناول حاصرات بيتا للسيطرة عليه، وللنوبات (حاليًا مرتين أسبوعيًا)، أتناول دواء أليغرو. تتدهور جودة حياتي ومتعتي بها عامًا بعد عام، وفكرة التخلص منه عن طريق لقاح تبدو خيالية. عندما تُجرب كل علاجات الصداع النصفي، يصعب عليك أن تأمل في عيش حياة خالية من الهموم مجددًا. أعيش جنوب ميونخ، وسأكون أول من يتطوع للمشاركة في التجارب فورًا.
أستاذ غوبل، من الرائع وجود أطباء مثلك يواصلون البحث وفهم المعنى الحقيقي لألم الشقيقة - شكرًا لك! كنتُ أيضًا في عيادتك عام ٢٠١٠، وتحسنت حالتي كثيرًا مع الأدوية التي وُصفت لي حديثًا؛ فقد انخفضت نوبات الشقيقة وخفّ الألم. وأصبحتُ أتمتع بنوعية حياة شبه طبيعية. أما الآن، فقد عادت النوبات لتصبح أكثر تواترًا. عانيتُ من ألم مبرح لمدة ثلاثة أيام وليلة، ولم تُجدِ تحاميل نوفالجين ولا دواء ماكسالت نفعًا. سيكون من الرائع لو نجح اللقاح. وقد
تم تقييمي منذ ذلك الحين بأنني أعاني من إعاقة بنسبة ٥٠٪، وهي معلومة قد تكون مهمة لمرضى الشقيقة الآخرين.
سأكون متاحاً على الفور. لن تهم الآثار الجانبية وما إلى ذلك، لأنها لا يمكن أن تكون سيئة مثل المعاناة من الصداع والصداع النصفي على مدار 24 ساعة تقريباً طوال أيام الأسبوع
أودّ بشدة التطوع كمتطوعة في التجارب السريرية. أعاني من الصداع النصفي منذ 25 عامًا، وجرّبت العديد من العلاجات دون جدوى تُذكر. خوفًا من عدم قدرتي على رعاية طفلتي ونقل هذا المرض اللعين إليها، بقيتُ بلا أطفال. في بعض الأحيان، يُسيطر عليّ المرض لدرجة أنني أفقد الرغبة في العيش.
مرحباً أستاذ غوبل،
أعاني من الصداع النصفي منذ أن كان عمري عشر سنوات، أي منذ 45 عاماً.
وبما أنني سأكون في عيادتكم ابتداءً من الثاني من يونيو، فسيسعدني المشاركة كمتطوع في الدراسة!
يا له من أمر رائع!
أعاني من الصداع يومياً، وتصيبني نوبات صداع نصفي حادة كل 3-5 أيام.
أخشى أن أنقل هذا المرض إلى أطفالي، وأنا حالياً بلا أطفال.
أتمنى للجميع الكثير من الأمل ووقتًا خاليًا من الألم.
لأن الأمل هو آخر ما يموت.
أعاني من الصداع النصفي منذ ثلاثين عامًا، عادةً لمدة تتراوح بين ١٢ و١٩ يومًا شهريًا. إذا كان هذا اللقاح فعالًا حقًا وحصلت عليه، فسيتحقق حلمٌ طال انتظاره وتنتهي معاناتي. سيكون ذلك إنجازًا طبيًا عظيمًا، لطالما تاق إليه الكثيرون ممن يعانون من الصداع النصفي.
لأعيش أخيراً بدون ألم، سأجعل نفسي متاحاً على الفور
أعاني من الصداع النصفي منذ 15 عامًا، في البداية كان يقتصر على فترة الحيض، ثم أصبح الطقس عاملًا محفزًا، والآن أعاني منه بشكل شبه دائم. سأجربه فورًا للتخلص نهائيًا من هذا الألم؛ فجودة حياتي في أسوأ حالاتها.
أعاني من الصداع النصفي منذ 30 عامًا. لطالما تناولت دواء كافيرجوت، وهو مثالي لحالتي! لم تُجدِ أنواع التريبتانات المختلفة نفعًا. لم أُعانِ قط من أي آثار جانبية للإرغوتامين. طبيبي في النمسا لم يعد مُصرَّحًا له بوصف الإرغوتامين. أنا في أمسّ الحاجة للمساعدة لأن كافيرجوت هو الحل الوحيد لي. أتناول الآن دواء يوميتان، ولكنه أيضًا لا يُخفف الألم. أحتاج إلى ثلاث أقراص لتخفيفه، ثم يعود. مع كافيرجوت، أحتاج فقط إلى نصف تحميلة. أرجوكم، من يستطيع مساعدتي؟
أعاني من الصداع النصفي منذ 35 عامًا، بمعدل يصل إلى 15 نوبة شهريًا. وقد منحني هذا التقرير الأمل. وسأشارك بكل سرور في دراسة مماثلة.
أعاني من الصداع النصفي المصحوب بهالة منذ أن كان عمري عشر سنوات، حيث تصل نوباتي إلى عشرين نوبة شهريًا. قبل أربع سنوات، خضعت لعملية جراحية لإغلاق الثقبة البيضوية المفتوحة، وأتناول دواء بلافيكس. منذ ذلك الحين، اختفت الهالة تمامًا. مع ذلك، أعاني حاليًا من نوبتين إلى ثلاث نوبات صداع نصفي بدون هالة أسبوعيًا، وأتناول دواء أليغرو. أخشى ألا أتمكن من تناول بلافيكس بعد الآن، لأني سأعجز عن العمل (على الكمبيوتر) بسبب اضطرابات بصرية وأعراض أخرى (صعوبة في الكلام) تصل إلى عشرين مرة يوميًا.
سيكون اللقاح رائعًا، فهو سيمكنني من التعامل مع مستويات التوتر الطبيعية، وسيكون بمثابة حلم يتحقق.
سأتطوع للمشاركة في التجارب السريرية.
أعاني من الصداع النصفي منذ سن الخامسة عشرة، وأود بشدة المشاركة في هذه الدراسة ومتابعة نتائجها. أعيش في برلين.
عزيزي الأستاذ غوبل،
يسعدني جدًا أن أقرأ عن التزامكم تجاه مرضى الشقيقة.
أعاني (52 عامًا) من الشقيقة منذ 46 عامًا، وتصل نوباتها إلى 20 نوبة شهريًا. متعتي بالحياة محدودة للغاية!
أعتقد أن ابنتي (15 عامًا) هي الوحيدة التي تُبقيني صامدة، وأشعر بذنب كبير تجاهها لأنني نقلت إليها الشقيقة. أصيبت بأول نوبة لها وهي في الرابعة من عمرها!
للأسف، النمسا دولة نامية فيما يتعلق بالشقيقة. ورغم وجود عيادة للصداع في مستشفى فيينا العام (AKH)، إلا
أنه من المستحيل الحصول على موعد (مدة الانتظار سنتان!).
أنا شخصيًا أتناول دواء ريلباكس 40 ملغ، لكن لا يمكنني تناول أكثر من 10 أقراص شهريًا.
تقريركم "التطعيم بـ CGRP ضد الصداع النصفي" رائع ويعطي الأمل - ربما ليس بالنسبة لي بعد الآن،
ولكن ابنتي (15 عامًا) قد تتمكن من تحسين حياتها من خلاله.
أتمنى لكم كل التوفيق
وأرسل لكم أطيب التحيات من فيينا.
كل من يُثيرون المشاعر ضد صناعة الأدوية (وهذا يحدث كثيراً) عليهم أن يختبروا معنى الأمل عندما يُعانون من الصداع النصفي بشكل شبه يومي ولا يستطيعون تناول التريبتانات إلا لعشرة أيام فقط. أنا حالياً في فترة راحة من التريبتانات وأُعاني معاناة شديدة. إنّ مجرد التفكير في التعافي، حتى لو كان بعد بضع سنوات، أمرٌ رائع حقاً. شكراً جزيلاً لكل من يعمل على تطوير هذا الدواء!
أستاذي العزيز غوبل،
بعد أكثر من ثلاثين عامًا من المعاناة مع الصداع النصفي، يمنحني تقريرك الأمل في التخلص منه قريبًا. التخلص من نوبات الصداع النصفي التي سيطرت على حياتي - وحياة ملايين غيري - لفترة طويلة جدًا. أرشحك لجائزة نوبل في الطب. :-)) شكرًا جزيلًا لك على سنوات تفانيك!
حتى الآن، لم تشكو من معاناتها سوى النساء، لكنها تصيب الرجال أيضاً.
أعاني من الصداع النصفي منذ 39 عاماً. أعمل لحسابي الخاص وأعمل باستمرار، لذا فإن يوم الأحد هو يوم إجازتي الوحيد. في
أيام الأحد، عادةً ما أبقى في الفراش أعاني من نوبات الألم. أما خلال الأسبوع، فأجد سريراً في شركتي ألجأ إليه عند حدوث النوبات. أستمتع بالحياة كثيراً، لذا أود التطوع للمشاركة في هذه التجربة.
عزيزي البروفيسور غوبل،
لقد زرت عيادتكم في يناير/فبراير 2015، وأشعر بتحسن كبير الآن. وللتخلص
نهائياً من الصداع النصفي، يسعدني جداً التطوع للمشاركة في تجربة سريرية.
أعاني من الصداع النصفي الحاد منذ الطفولة، وسأتطوع فوراً للمشاركة في هذه الدراسة..
وصلتُ للتو إلى المنزل من عند عائلتي، وكنا نتحدث عن هذا الأمر أيضًا... لقد جربتُ كل شيء لأكثر من 15 عامًا... عمري الآن 37 عامًا، ومنذ شهور وأنا أعاني من نوبات هلع قبل النوبة التالية. لا أعرف كيف كنتُ أعيش بدون دواء سوماتريبتان المعجزة؟ إذا احتجتُ فقط إلى 4 أو 5 حبات منه خلال 72 ساعة، تُعتبر النوبة "جيدة". سأفعل أي شيء تقريبًا لأُشفى. بل سأتطوع بكل سرور لأكون متطوعة في تجربة سريرية!
سيكون ذلك بمثابة حلم يتحقق!
أبلغ من العمر 41 عامًا وأعاني من الصداع النصفي منذ الطفولة. لسوء الحظ، بدأت نوبات الهلع قبل خمس سنوات، وأعاني الآن أيضًا من الاكتئاب. ولأنني أعاني أيضًا من الربو، لا أستطيع استخدام حاصرات بيتا للوقاية. بل إنني مستعدة للتطوع لأكون فأرة تجارب دون تردد.
سيكون ذلك ثورياً! لقد عانيت من الصداع النصفي لمدة 65 عاماً - سأشارك في دراسة على الفور.
مرحباً، أود المشاركة في الدراسة فوراً. أعاني من الصداع النصفي منذ 53 عاماً، وهو متكرر جداً هذه الأيام. مع خالص التحيات، شارلوت ماسلونكا
إذا نجح هذا على المدى الطويل، فسيكون نعمةً لجميع من يعانون من الصداع النصفي...
لقد جربتُ بالفعل الكثير من الأشياء، من الطب التقليدي إلى أساليب العلاج البديلة،
وكلها دون جدوى... لم يُجنِ سوى خسارة مالية كبيرة.
سأشارك في دراسة فورًا... أعاني من الصداع النصفي منذ 13 عامًا، وأعاني منه الآن بشكل شبه يومي.
سيكون ذلك رائعًا! نعمةٌ عظيمةٌ للعديد من المصابين الذين تتأثر جودة حياتهم سلبًا!
بعد 45 عامًا من المعاناة من الصداع النصفي، حيث أعاني حاليًا من 13 إلى 16 يومًا من الصداع النصفي شهريًا، أتمنى بشدة استخدامه!
حياة بلا ألم الصداع النصفي؟ هذا يفوق خيالي... جنة على الأرض!
سيكون هذا بمثابة ثورة حقيقية. أتمنى بشدة المشاركة في هذه الدراسة. أعاني من هذه المشكلة منذ أكثر من 35 عامًا!
سيكون ذلك بمثابة حلم يتحقق – بعد 60 عامًا من تجربة جميع أنواع الأدوية…
يرجى إطلاعنا على آخر المستجدات بشأن هذه الطريقة – شكرًا لكم.
عزيزي الأستاذ غوبل،
سيكون ذلك رائعًا. أعاني من الصداع النصفي المزمن، وسأتطوع فورًا للمشاركة في التجارب السريرية.
أتمنى من كل قلبي أن يُحقق هذا الدواء نجاحًا لجميع مرضى الصداع النصفي، كما نتمنى جميعًا!
يبدو الأمر جيداً لدرجة يصعب تصديقها... سأكون متاحاً على الفور..
بعد 54 عاماً من المعاناة من الصداع النصفي، كان هذا بمثابة الفوز بالجائزة الكبرى!
أستاذ غوبل،
سررتُ بقراءة ذلك. آمل ألا تكون هناك عقبات بيروقراطية كثيرة يجب تجاوزها حتى يتسنى تطبيق علاج الحقن في أقرب وقت ممكن. بصفتي مريضًا سابقًا في عيادتكم، أُقدّم نفسي كمتطوع للتجربة. لم أشعر بأي تحسن يُذكر من البوتوكس.
سأتطوع للمشاركة في التجارب فوراً. بعد 42 عاماً من المعاناة من الصداع النصفي، أشعر بإرهاق شديد
سأكون متاحاً على الفور. سيكون حلماً يتحقق بالنسبة لي أن أتخلص من الألم مجدداً.
سأشارك فوراً!!! حلمٌ أصبح حقيقة... أخيراً سأعيش بلا ألم!
43 عاماً من المعاناة في رأسي، وبالتالي في حياتي. أتمنى بشدة المشاركة في هذه الدراسة.
أخيرًا، التخلص من الألم، ستكون هذه هدية رائعة، سأجربها على الفور!
هذا يستحق جائزة نوبل!
يا
له من حلم،
لن أعاني من الصداع النصفي بعد الآن :-)
سيكون ذلك رائعاً! سأجربه فوراً!
لو نجحت هذه الطريقة فعلاً، وأصبح بإمكان المرء التخلص من الألم أو الحفاظ على صحته، لكان ذلك إنجازاً ثورياً. أعتقد أن كل من يعاني من الصداع النصفي سيتطوع فوراً للمشاركة في التجربة، وأنا منهم.
ثورة في علاج آلام الصداع النصفي. سأكون متاحاً على الفور.
سيكون ذلك بمثابة معجزة بعد 37 عاماً من المعاناة من الصداع النصفي!!!
سيكون ذلك رائعاً!
سيتحقق الحلم