تُعبّر العديد من مناطق الدماغ ذات الصلة بآلية حدوث الشقيقة، والجهاز الوعائي القحفي، والأم الجافية، والقرن الظهري للنخاع الشوكي، عن مستقبلات الإستروجين. وهذا يسمح بتعديل الاستجابة للمؤثرات المؤلمة. قد تحدث نوبات الشقيقة بالتزامن مع فترة الحيض. تُعدّ الشقيقة عامل خطر للإصابة بالسكتة الدماغية وغيرها من الأحداث الوعائية. توجد أدلة كثيرة تُشير إلى أن زيادة خطر الإصابة بالسكتة الدماغية الإقفارية يرتبط بكلٍ من الشقيقة بدون هالة والشقيقة مع هالة. ونظرًا لأن خطر الإصابة بالسكتة الدماغية قد يزداد أيضًا مع استخدام موانع الحمل الهرمونية، فإن مسألة خيارات الإدارة العملية تُعدّ بالغة الأهمية.
تصنيف الصداع النصفي وعلاقته بالحيض
لا يتضمن الإصدار الثالث الحالي من التصنيف الدولي لاضطرابات الصداع (ICHD3) [1]، كما في الإصدارات السابقة، قسمًا خاصًا بنوبات الصداع النصفي التي تحدث بالتزامن مع فترة الحيض في متن التصنيف. ولم يقدم الإصدار الأول الصادر عام 1988 [2] أي معايير رسمية للصداع النصفي المرتبط بالحيض. ومع ذلك، حتى في هذا الإصدار الأول، أشار التعليق إلى أن بعض النساء يعانين من نوبات صداع نصفي بدون هالة حصريًا أثناء الحيض. وقد أُطلق على هذه الحالة اسم "الصداع النصفي الحيضي". وكان يُستخدم هذا المصطلح فقط إذا حدثت 90% على الأقل من النوبات في الفترة الممتدة من يومين قبل الحيض إلى آخر يوم منه. وفي الإصدار الثاني من التصنيف الدولي لاضطرابات الصداع عام 2004 [3]، تم تعريف نوعين فرعيين من الصداع النصفي المرتبط بالحيض لأول مرة في الملحق. ويشير ما يُسمى "الصداع النصفي الحيضي الخالص" إلى النوبات التي تحدث حصريًا بالتزامن مع الحيض. في المقابل، يتميز ما يُسمى بـ"الصداع النصفي المرتبط بالحيض" بنوبات تحدث في أوقات أخرى من الدورة الشهرية. وكلا النوعين يُعدّان مجموعتين فرعيتين من الصداع النصفي بدون هالة. يصف الملحق الخاص بالتصنيف الدولي لاضطرابات الصداع معايير البحث لأنواع الصداع التي لم يتم التحقق من صحتها بشكل كافٍ من خلال الدراسات العلمية. تشير كل من خبرة أعضاء لجنة تصنيف الصداع والمنشورات ذات الجودة المتفاوتة إلى وجود هذه الأنواع المدرجة في الملحق، والتي يمكن اعتبارها أمراضًا متميزة. ومع ذلك، يلزم توفير المزيد من الأدلة العلمية قبل قبولها رسميًا. إذا تحقق ذلك، يمكن دمج هذه التشخيصات الواردة في الملحق في متن التصنيف الرئيسي في المراجعة القادمة.
حتى في الطبعة الثالثة من التصنيف الدولي لاضطرابات الصداع (ICD) لعام ٢٠١٨، لا يزال مصطلحا "الصداع النصفي الحيضي البحت" و"الصداع النصفي المرتبط بالحيض" مُدرجين فقط في الملحق. ويشترط لتشخيص كلا النوعين حدوث نوبات الصداع النصفي في اليوم الأول أو الثاني من الدورة الشهرية (أي من اليوم -٢ إلى اليوم +٣) في دورتين شهريتين على الأقل من أصل ثلاث دورات شهرية (الجدول ١، الشكل ١). ومع ذلك، تم توسيع المعايير لتشمل نوعًا فرعيًا مصحوبًا بهالة، على الرغم من أن نوبات الصداع النصفي الحيضي عادةً ما تحدث بدون هالة. وبالتالي، تم تعريف الصداع النصفي الحيضي البحت مع الهالة وبدونها، وكذلك الصداع النصفي المرتبط بالحيض مع الهالة وبدونها. وعند دمج الصداع النصفي الحيضي البحت والصداع النصفي المرتبط بالحيض، يُستخدم مصطلح "الصداع النصفي الحيضي" كمصطلح عام [٤].
الجدول 1. معايير التشخيص ICHD-3 للصداع النصفي داخل وخارج فترة الحيض
———————————————————————————
أ1.1.1 الصداع النصفي المرتبط بالحيض فقط بدون هالة
- النوبات لدى المرأة في فترة الحيض 1 ، والتي تستوفي الصداع النصفي بدون هالة
- تحدث النوبات حصريًا في اليوم 1 ± 2 (أي من اليوم -2 إلى +3) من الدورة الشهرية الأولى في دورتين على الأقل من أصل 3 دورات شهرية، وليس في أي وقت آخر من الدورة.
أ1.1.2 الصداع النصفي المرتبط بالحيض بدون هالة
- النوبات التي تصيب المرأة في فترة الحيض والتي تستوفي معايير 1.1 الصداع النصفي بدون هالة بالإضافة إلى المعيار ب أدناه
- تحدث النوبات في اليوم 1 ± 2 من الدورة الشهرية ( أي اليوم -2 إلى +3) في دورتين على الأقل من أصل ثلاث دورات شهرية، ولكن أيضًا في أوقات أخرى من الدورة.
أ1.1.3 الصداع النصفي غير المرتبط بالحيض بدون هالة
- النوبات التي تصيب المرأة في فترة الحيض والتي تستوفي معايير 1.1 الصداع النصفي بدون هالة بالإضافة إلى المعيار ب أدناه.
- تستوفي المعيار B للصداع النصفي المرتبط بالحيض بدون هالة أو الصداع النصفي المرتبط بالحيض بدون هالة
———————————————————————————
A1.2.0.1 الصداع النصفي المرتبط بالحيض فقط مع هالة
- النوبات لدى المرأة في فترة الحيض 1 ، والتي تستوفي معايير 1.2 الصداع النصفي المصحوب بهالة والمعيار ب أدناه
- تحدث النوبات في اليوم 1 ± 2 من الدورة الشهرية (أي من اليوم -2 إلى +3) في دورتين على الأقل من أصل ثلاث دورات شهرية، ولكن أيضًا في أوقات أخرى من الدورة.
A1.2.0.2 الصداع النصفي المصاحب للحيض مع هالة
- النوبات التي تصيب المرأة في فترة الحيض والتي تستوفي معايير 1.2 للصداع النصفي المصحوب بهالة والمعيار ب أدناه
- تحدث النوبات في اليوم 1 ± 2 من الدورة الشهرية ( أي اليوم -2 إلى +3) في دورتين على الأقل من أصل ثلاث دورات شهرية، ولكن أيضًا في أوقات أخرى من الدورة.
A1.2.0.3 الصداع النصفي غير المرتبط بالحيض المصحوب بهالة
- النوبات التي تصيب المرأة في فترة الحيض والتي تستوفي معايير 1.2 للصداع النصفي المصحوب بهالة والمعيار ب أدناه
- تستوفي المعيار B للصداع النصفي المرتبط بالحيض فقط مع هالة أو A1.2.0.2 الصداع النصفي المرتبط بالحيض مع هالة
———————————————————————————
لأغراض التصنيف الدولي لاضطرابات الصداع (ICHD-3)، يُعتبر الحيض نزيفًا رحميًا ناتجًا عن الدورة الشهرية الطبيعية أو عن التوقف عن استخدام البروجستينات الخارجية، كما هو الحال مع موانع الحمل الفموية المركبة والعلاج الهرموني التعويضي الدوري (الشكل 1). ويُعد التمييز بين الصداع النصفي المرتبط بالحيض فقط دون هالة والصداع النصفي المرتبط بالحيض دون هالة أمرًا مهمًا وفقًا لتصنيف ICHD-3، لأن الوقاية الهرمونية تكون أكثر فعالية في الحالة الأخيرة [1].
أفادت أكثر من 50% من النساء المصابات بالصداع النصفي بوجود ارتباط بين الدورة الشهرية والصداع النصفي [5]. ويختلف معدل الانتشار بين الدراسات نظرًا لاختلاف معايير التشخيص. يتراوح معدل انتشار الصداع النصفي المصاحب للدورة الشهرية بدون هالة بين 7% و14% لدى مريضات الصداع النصفي، بينما يتراوح معدل انتشار الصداع النصفي المصاحب للدورة الشهرية بدون هالة بين 10% و71% لدى مريضات الصداع النصفي. وتعاني واحدة من كل ثلاث إلى خمس مريضات بالصداع النصفي من نوبة صداع نصفي بدون هالة بالتزامن مع الدورة الشهرية [5]. تميل العديد من النساء إلى المبالغة في تقدير العلاقة بين الدورة الشهرية ونوبات الصداع النصفي؛ ولأغراض البحث، يتطلب التشخيص توثيقًا استباقيًا لثلاث دورات شهرية على الأقل، مدعومًا بتطبيق خاص بالصداع النصفي أو سجلات يومية [1].
قد تختلف آليات الصداع النصفي تبعًا لما إذا كان نزيف بطانة الرحم يحدث نتيجةً للدورة الشهرية الطبيعية أو نتيجةً للتوقف عن استخدام البروجستينات الخارجية (كما هو الحال مع حبوب منع الحمل المركبة والعلاج الهرموني التعويضي الدوري). تنتج الدورة الشهرية الطبيعية عن تغيرات هرمونية معقدة في محور الغدة النخامية-الوطائية-المبيضية التي تحفز الإباضة، والتي يتم تثبيطها باستخدام حبوب منع الحمل المركبة. لذلك، ينبغي دراسة هاتين المجموعتين الفرعيتين من الناحية الفيزيولوجية المرضية بشكل منفصل، على الرغم من أن المعايير التشخيصية لا يمكن تمييزها بشكل متبادل.
تشير الأدلة إلى أن نوبات الصداع النصفي المرتبط بالحيض قد تُثار بانخفاض مستوى هرمون الإستروجين، على الأقل لدى بعض النساء، مع العلم أن التغيرات الهرمونية أو الكيميائية الحيوية الأخرى في هذه المرحلة من الدورة الشهرية قد تكون ذات صلة أيضًا [4]. إذا ارتبط الصداع النصفي المرتبط بالحيض فقط، أو الصداع النصفي المصاحب للحيض، بانخفاض مستوى هرمون الإستروجين الخارجي، فينبغي تشخيص الحالتين معًا: الصداع النصفي المرتبط بالحيض فقط بدون هالة، أو الصداع النصفي المصاحب للحيض بدون هالة وصداع انخفاض مستوى الإستروجين. وقد يتغير ارتباط هذه الحالة بالحيض خلال فترة حياة المرأة الإنجابية.
تأثير الهرمونات على الصداع
أُدرج تأثير الهرمونات على الصداع في القسم الرئيسي "الصداع الثانوي" في الطبعة الثانية (ICHD-2) من التصنيف الدولي لاضطرابات الصداع لعام 2004 [3]. وتتعلق المعايير بالصداع الذي ظهر حديثًا نتيجةً لتناول الهرمونات، أو الصداع الموجود مسبقًا والذي تفاقم بسببها. وتشترط هذه المعايير تحسن الصداع بعد التوقف عن تناول الهرمونات، أو في حالة الصداع الموجود مسبقًا، عودة نمطه السابق.
اشترطت الطبعة الثالثة من التصنيف الدولي لاضطرابات الصداع (ICHD-3) لعام 2018 [1] وجود صداع لمدة 15 يومًا على الأقل شهريًا لتشخيص الصداع المرتبط بالهرمونات الخارجية. ويشترط تشخيص صداع انسحاب الإستروجين وفقًا للتصنيف الدولي لاضطرابات الصداع (ICHD-3) أن يبدأ الصداع في غضون 5 أيام من التوقف عن تناول الإستروجين إذا كانت المرأة قد تناولته لمدة ثلاثة أسابيع على الأقل.
الإستروجين والصداع النصفي
في عام ١٩٧٢، وصف سومرفيل كيف أن الحقن العضلي لإستراديول فاليرات، وهو إستر أولي لـ ١٧β-إستراديول، قبل الحيض بفترة وجيزة، يمكن أن يؤخر بدء نوبة الصداع النصفي المرتبطة بالحيض [٦]. وتم تحديد تركيز عتبة للإستراديول ١٧β في الدورة الدموية يتراوح بين ٤٥ و٥٠ بيكوغرام/مل، والذي يمكن أن يؤدي انخفاضه إلى بدء نوبة الصداع النصفي. ولوحظت هذه العتبة أيضًا لدى النساء بعد انقطاع الطمث اللواتي يخضعن للعلاج الهرموني البديل باستخدام ١٧β-إستراديول عن طريق الحقن العضلي. وبناءً على هذه البيانات، طُرحت فرضية مفادها أن نوبات الصداع النصفي خلال فترة الحيض تُحفز بانخفاض مستوى الإستروجين. كما افترض الباحثون أن التقلبات الفسيولوجية للإستروجين تلعب دورًا في آلية حدوث الصداع النصفي. وقد دعمت هذه الفرضية ملاحظة وجود قابلية خاصة للإصابة بنوبات الصداع النصفي خلال انخفاض مستوى الإستروجين في المرحلة الأصفرية المتأخرة. ومع ذلك، لم يتم إثبات وجود اختلافات في الحد الأقصى أو المتوسط اليومي لتركيزات هرمون الاستروجين خلال دورات الإباضة لدى مرضى الصداع النصفي مقارنة بالمجموعات الضابطة الصحية [4، 7].
الإستروجين والجهاز العصبي
يُعدّ 17β-إستراديول أهمّ هرمون استروجين داخلي المنشأ [8]. يدخل هذا الهرمون إلى الجهاز العصبي المركزي عبر الانتشار السلبي من خلال الحاجز الدموي الدماغي. مع ذلك، يُمكن أيضًا تصنيعه محليًا في الدماغ من الكوليسترول أو من سلائف مُؤرْمَتة بواسطة إنزيم الأروماتاز، حيث يعمل كهرمون عصبي ستيرويدي. وتتوسط التأثيرات الفيزيولوجية تنشيط مستقبلات استروجينية مختلفة، ولا سيما مستقبلات الاستروجين ألفا (ERα)، ومستقبلات الاستروجين بيتا (ERβ)، ومستقبلات الاستروجين المقترنة بالبروتين G-1 (GPER/GPR30) [9].
تُمارس هرمونات الإستروجين تأثيراتها البيولوجية في الجهاز العصبي المركزي من خلال آليات خلوية جينومية أو غير جينومية. وهذا بدوره يُمكن أن يُغير النقل العصبي ووظائف الخلايا. كما يُمكن لسلاسل الإشارات داخل الخلايا أن تُعدل التفاعلات الإنزيمية، وموصلية قنوات الأيونات، واستثارة الخلايا العصبية [4].
تُعبر العديد من مناطق الدماغ المشاركة في الفيزيولوجيا المرضية للصداع النصفي عن مستقبلات الإستروجين. وينطبق هذا بشكل خاص على منطقة ما تحت المهاد، والمخيخ، والجهاز الحوفي، ونوى الجسر، والمادة الرمادية المحيطة بالمسال الدماغي. كما تُعبر مستقبلات الإستروجين في القشرة الدماغية، مما يؤثر على حساسية الألم واردًا وصادرًا. ويُعبر الجهاز الوعائي القحفي، والأم الجافية، والقرن الظهري للنخاع الشوكي أيضًا عن مستقبلات الإستروجين، مما يؤثر على المحفزات المؤلمة [4، 8، 9].
لم تُظهر دراسات الارتباط على مستوى الجينوم أي علاقة بين تعدد أشكال مستقبلات الإستروجين وزيادة خطر الإصابة بالصداع النصفي. ومع ذلك، تم تحديد تعدد أشكال نوكليوتيدي واحد في جين SYNE1 مرتبط بالصداع النصفي المرتبط بالحيض [10].
يمكن تنشيط الجهاز السيروتونيني بواسطة هرمون الإستروجين، مما قد يكون له تأثير وقائي ضد نوبات الصداع النصفي [11]. كما يمكن للإستروجين أن يزيد من التأثير المحفز للجلوتامات. وهذا قد يفسر زيادة احتمالية ظهور هالة الصداع النصفي خلال فترات ارتفاع تركيز الإستروجين، كما هو الحال أثناء الحمل أو عند تناول الهرمونات الخارجية.
يُمكن للإستروجين تعديل نظام حمض غاما-أمينوبيوتيريك (GABA)، الذي له تأثير مثبط في الجهاز العصبي [12]. أما البروجسترون، الذي يُنتج بشكل رئيسي من الجسم الأصفر في المبيضين، بالإضافة إلى مستقلبه ألوبيرغنانولون، فيُمكنه تعزيز نشاط GABAergic وبالتالي إحداث تأثير مسكن للألم.
يمكن للإستروجينات أيضًا تعديل نظام الأفيونيات الداخلي عن طريق زيادة تخليق الإينكيفالين [13]. وبناءً على ذلك، قد يرتبط انخفاض مستويات الإستروجين والبروجسترون خلال المرحلة الأصفرية المتأخرة بانخفاض تنشيط نظام الأفيونيات، مما يؤدي إلى زيادة حساسية الألم. وقد أظهرت الدراسات التي تناولت حساسية الألم خلال المراحل المختلفة من الدورة الشهرية زيادةً في الحساسية خلال المرحلة الأصفرية، لا سيما لدى النساء اللواتي يعانين من أعراض ما قبل الحيض [14]. كما تحفز التركيزات العالية من الإستروجين إنتاج ناقلات عصبية وببتيدات عصبية أخرى مثبطة للألم، مثل الببتيد العصبي Y والبرولاكتين والفازوبريسين، والتي قد تلعب دورًا في تطور الصداع النصفي [4].
الأوكسيتوسين والصداع النصفي
يُنتَج هرمون الأوكسيتوسين، وهو ببتيد عصبي، في منطقة ما تحت المهاد، وله تأثيرات واسعة على الجهاز العصبي المركزي، لا سيما في تنظيم المزاج والسلوك. كما يؤثر على آلية الجسم في التحكم بالألم، وقد يكون له تأثير وقائي من الصداع النصفي [4]. وتزداد مستويات الأوكسيتوسين أيضًا خلال فترات ارتفاع تركيز هرمون الإستروجين، إذ يؤدي الإستروجين إلى زيادة إنتاج الأوكسيتوسين في منطقة ما تحت المهاد ومناطق أخرى من الدماغ، وخاصة في النواة الذيلية للعصب ثلاثي التوائم [15]. وتُظهر النساء اللواتي يعانين من الصداع النصفي المرتبط بالدورة الشهرية انخفاضًا في عتبة الألم خلال الفترة الخالية من الهرمونات عند تناول موانع الحمل الهرمونية المركبة، أي في وقت انخفاض تركيز هرمون الإستروجين [16].
ترتبط الآلية المرضية للصداع النصفي بزيادة النشاط الحسي للألم في القشرة الدماغية ضمن الجهاز الحسي للألم ثلاثي التوائم الوعائي. ويؤدي ذلك إلى توسع الأوعية الدموية داخل الجمجمة والتهاب السحايا [15]. وقد يُحفز التنشيط الموضعي لمستقبلات الإستروجين في العقدة ثلاثية التوائم نوبات الصداع النصفي. وتمتلك النساء عددًا أكبر من مستقبلات الإستروجين في العقدة ثلاثية التوائم مقارنةً بالرجال [17]. ويمكن للإستروجينات أن تؤثر بشكل حاد على توتر الأوعية الدموية عن طريق تثبيط قنوات الكالسيوم في العضلات الملساء [18]. كما يمكن للإستروجينات أن تُنشط الاكتئاب القشري المنتشر (CSD)، وهو استقطاب عصبي قشري يُعتبر سمة مميزة للصداع النصفي المصحوب بهالة [19]. وتزيد المستويات العالية من الإستروجين من قابلية الإصابة بالاكتئاب القشري المنتشر، بينما يُقلل نقص الإستروجين من هذه القابلية. وهذا قد يُفسر سبب كون نوبات الصداع النصفي خلال فترة الحيض أقل ارتباطًا بالهالة [1].
الإستروجينات والببتيدات المرتبطة بجين الكالسيتونين (CGRP)
يُعدّ إطلاق الببتيد المرتبط بجين الكالسيتونين (CGRP) خطوةً حاسمةً في الفيزيولوجيا المرضية للصداع النصفي. إذ يُمكن أن يُؤدي تحفيز العقدة الثلاثية التوائم إلى إطلاق CGRP والمادة P في مجرى الدم الدماغي [20]. يُنشّط CGRP آليات الألم في الأم الجافية، والعقدة الثلاثية التوائم، ومجمع النواة الثلاثية التوائم العنقية، والمهاد، والمادة الرمادية المحيطة بقناة سيلفيوس، وغيرها من المواقع [20]. يُمكن أن تُثبّط التريبتانات كلاً من الأعراض السريرية للصداع النصفي وإطلاق CGRP [21]. قد تُحفّز حقن CGRP نوبةً لدى مرضى الصداع النصفي [22]، بينما لا يحدث ذلك لدى الأصحاء. تتوفر الآن الأجسام المضادة وحيدة النسيلة التي تستهدف على وجه التحديد CGRP كربيطة (إيبتينيزوماب، فريمانيزوماب، وغالكانيزوماب) أو مستقبل CGRP (إيرينوماب) للعلاج الوقائي للصداع النصفي العرضي والمزمن [23، 24]. وقد أثبتت التجارب السريرية المضبوطة فعاليتها وتحملها الجيد.
تكون مستويات الببتيد المرتبط بجين الكالسيتونين (CGRP) أعلى لدى النساء منها لدى الرجال [25]. كما ترتفع هذه المستويات أثناء الحمل ومع استخدام موانع الحمل الهرمونية المركبة. وتتفاوت مستوياته خلال فترة انقطاع الطمث [26]. ويُعبر عن مستقبلات CGRP والإستروجين في نفس مناطق الدماغ. ويمكن للإستروجين أن يُعدّل إنتاج CGRP في الخلايا العصبية الثلاثية التوائم. وقد أظهرت التجارب أن إعطاء الإستروجين الخارجي يؤدي إلى انخفاض مستويات CGRP [27]. وخلال فترة ما بعد انقطاع الطمث، قد ترتفع مستويات CGRP بينما تنخفض تركيزات الإستروجين [28].
يمكن أن يُسبب الببتيد العصبي P، وهو ببتيد وعائي فعال، التهابًا عصبيًا في السحايا مرتبطًا بالصداع النصفي [28]. ويمكن أن يُقلل إعطاء الإستروجين من مستويات الببتيد العصبي P في البلازما. باختصار، يُمكن للإستروجين أن يُعدّل كلاً من الببتيد المرتبط بجين الكالسيتونين (CGRP) والببتيد العصبي P من خلال تأثيرات مثبطة. وبالتالي، يُوفر الإستروجين آلية وقائية ضد الالتهاب العصبي [28]. علاوة على ذلك، يُمكن للإستروجين أن يُثبط التأثير المُنشط للبروجسترون على كلٍ من الببتيد المرتبط بجين الكالسيتونين (CGRP) والببتيد العصبي P. وهذا يُشير إلى أن الجمع بين الإستروجين والبروجسترون له تأثير مُثبت على إطلاق كلٍ من الببتيد المرتبط بجين الكالسيتونين (CGRP) والببتيد العصبي P [4].
يُظهر مرضى الشقيقة ارتفاعًا في مستويات السيتوكينينات المُحفزة للالتهاب أثناء نوبات الشقيقة وبينها [29]. وتشير الدراسات التجريبية إلى أن الإستروجينات قد تُثبط جزيئات الالتهاب المنتشرة في الدم. إضافةً إلى ذلك، فإن لها تأثيرًا وقائيًا ضد الالتهاب الناجم عن البروستاجلاندينات. في المقابل، قد يؤدي نقص الإستروجين إلى زيادة الحساسية للبروستاجلاندينات وتنشيط الالتهاب العصبي عن طريق زيادة إفراز الببتيدات العصبية مثل CGRP والمادة P والنيوروكينين [30].
باختصار، تشير البيانات المتاحة إلى أن الإستروجين لا يمارس تأثيرًا وقائيًا مباشرًا على نوبات الصداع النصفي. مع ذلك، يمكن للإستروجين أن يؤثر بشكل غير مباشر على عوامل تنشيط وتثبيط الصداع النصفي. ونتيجة لذلك، قد يتم تثبيط بدء نوبات الصداع النصفي في الجهاز العصبي الوعائي. وفي الدورة الدموية للعصب ثلاثي التوائم، قد تنخفض الحساسية للصداع النصفي. ويمكن أن يؤدي انخفاض تركيز الإستروجين إلى خفض عتبة نوبات الصداع النصفي [4، 15].
الإستروجينات في الوقاية من الصداع النصفي المرتبط بالدورة الشهرية
قد تحدث نوبات الصداع النصفي لدى بعض المرضى حصرياً خلال فترة الحيض [1]. وقد تتميز هذه النوبات بخصائص ألم أكثر حدة بشكل ملحوظ (من حيث المدة والشدة والتفاقم مع النشاط البدني) وأعراض مصاحبة (مثل الغثيان والقيء والحساسية للضوء والصوت) مقارنة بنوبات الصداع النصفي التي تحدث خارج فترة الحيض.
قد يكون التحكم في تركيزات هرمون الإستروجين الطبيعية وسيلةً للوقاية من نوبات الصداع النصفي المرتبطة بالحيض. والهدف من ذلك هو تقليل التقلبات الهرمونية وانخفاض مستويات الإستروجين أثناء الحيض. ويستند هذا إلى ملاحظة أن قابلية الإصابة بنوبات الصداع النصفي خلال فترة ما قبل الحيض (اليومين -2 و+3 من الحيض) ترتبط بانخفاض مستويات الهرمونات [31].
بشكل أساسي، هناك نهجان متاحان لاستخدام الهرمونات في العلاج الوقائي للصداع النصفي المرتبط بالدورة الشهرية:
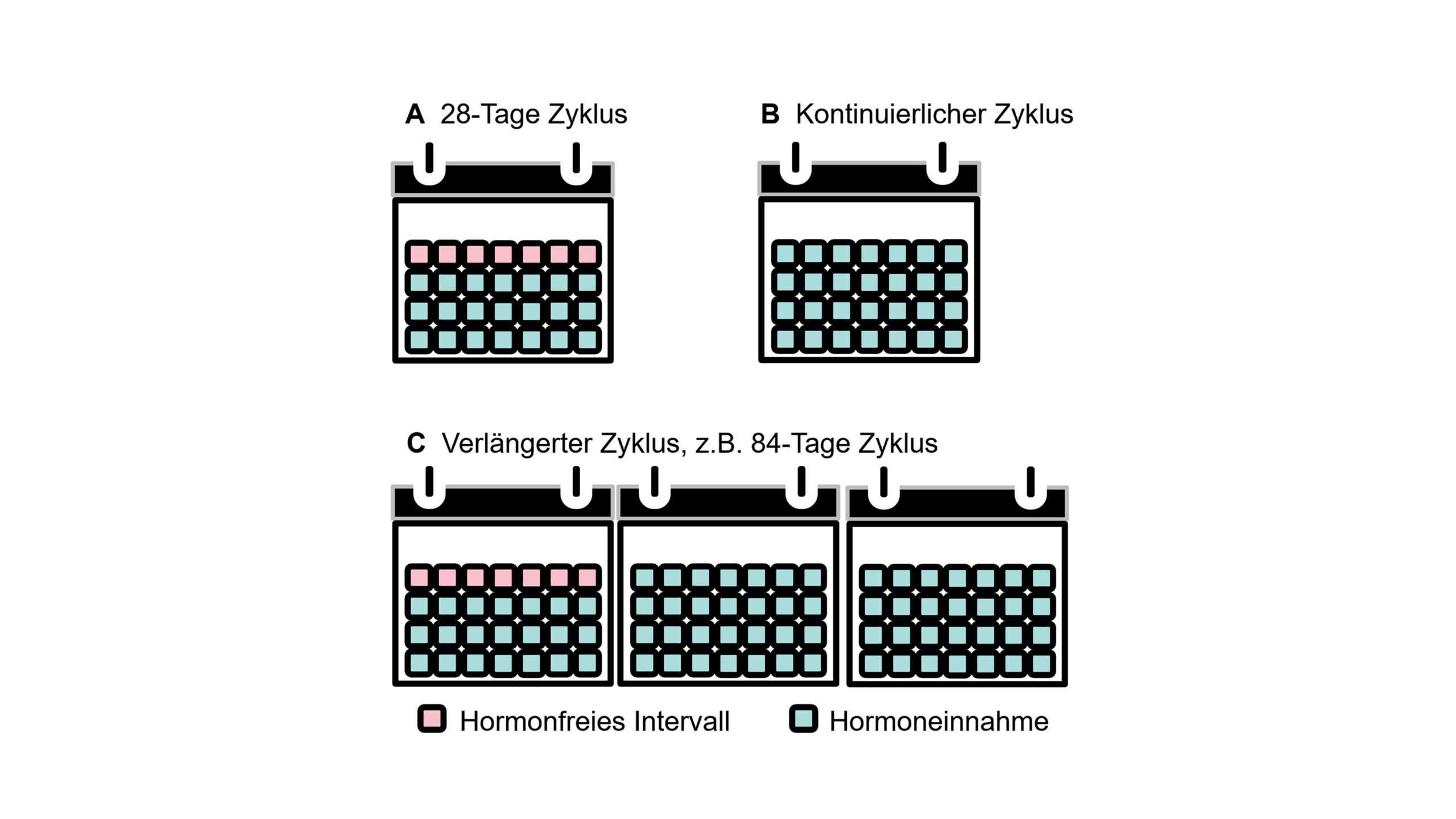
- يمكن استخدام موانع الحمل الهرمونية بأنظمة إعطاء مختلفة للإيثينيل إستراديول، وذلك تبعًا لمدة الفترة الخالية من الهرمونات. تشمل هذه الأنظمة النظام القياسي 21/7، والأنظمة الممتدّة المتغيرة، والأنظمة المستمرة دون فترات خالية من الهرمونات (الشكل 2). تشمل خيارات الإعطاء حبوب منع الحمل الهرمونية الفموية والحلقات المهبلية.
- بالإضافة إلى ذلك، يمكن استخدام مكملات الإستروجين غير المخصصة لمنع الحمل. ومن أمثلتها اللصقات الجلدية، والجل، والغرسات تحت الجلد. وتهدف هذه الوسائل إلى تعويض انخفاض مستويات الإستروجين خلال فترة ما قبل الحيض في حالات الصداع النصفي المرتبط بالحيض والصداع النصفي المرتبط بالحيض فقط.
البيانات المتعلقة باستخدام الهرمونات للوقاية من الصداع النصفي المرتبط بالدورة الشهرية محدودة للغاية ومتضاربة جزئيًا. ويكمن الأساس المنطقي في تعويض انخفاض هرمون الإستروجين الداخلي لدى المريضات المصابات بالصداع النصفي المرتبط بالدورة الشهرية فقط، واللاتي لديهن دورة شهرية منتظمة [4، 32، 33]. من جهة أخرى، يهدف الاستخدام المستمر لجرعات منخفضة إلى مواجهة التقلبات الهرمونية الفسيولوجية. ويهدف الاستخدام المشترك للإستروجين والبروجستين إلى تثبيت مستويات الهرمونات وتمكين منع الحمل [4، 32، 33]. وفيما يلي وصف لخيارات متنوعة للتأثير على الدورة الهرمونية الأنثوية لعلاج الصداع النصفي.
ديسوجيستريل (دواء يحتوي على البروجستين فقط)
أجرت أربع دراسات رصدية مفتوحة التسمية تقييمًا لتأثير ديسوجيستريل بجرعة 75 ميكروغرام يوميًا على النساء المصابات بالصداع النصفي المصحوب أو غير المصحوب بهالة [34-37]. تناولت النساء المشاركات في الدراسة الدواء إما كوسيلة لمنع الحمل أو لأسباب طبية، وليس للوقاية من الصداع النصفي. شملت الآثار الجانبية للديسوجيستريل تفاقم الصداع، وإطالة مدة النزيف، وظهور بقع دم، وحب الشباب. في المقابل، لا تزال الأدلة محدودة حول فعالية ديسوجيستريل في علاج الصداع النصفي لدى النساء المصابات به، سواءً المصحوب أو غير المصحوب بهالة. ونظرًا لانخفاض مخاطره على صحة القلب والأوعية الدموية، يمكن النظر في استخدام ديسوجيستريل لدى النساء المصابات بالصداع النصفي، سواءً المصحوب أو غير المصحوب بهالة، واللاتي لديهن عوامل خطر وعائية إضافية.
موانع الحمل الفموية المركبة
الأبحاث الحالية حول الاستخدام المطوّل لحبوب منع الحمل المركبة لدى النساء المصابات بالصداع النصفي محدودة [4، 32]. وحتى في هذه الحالة، لا تتوفر سوى دراسات رصدية مفتوحة، أُجريت على نساء تناولن الدواء لمنع الحمل أو لأسباب طبية، وليس للوقاية من الصداع النصفي. دراسة واحدة فقط استخدمت حبوب منع الحمل المركبة تحديدًا للوقاية من الصداع [38]. تشير البيانات المتاحة إلى فائدة محتملة للاستخدام طويل الأمد لحبوب منع الحمل الهرمونية المركبة لدى النساء المصابات بالصداع النصفي بدون هالة.
ديسوجيستريل مقابل الاستخدام المطول لحبوب منع الحمل المركبة
قارنت دراسات رصدية مفتوحة التأثيرَ لحبوب ديسوجيستريل الصغيرة مع الاستخدام المطوّل لحبوب منع الحمل الفموية المركبة في علاج الصداع النصفي بدون هالة. ووجدت دراسة أجراها موروتي وآخرون [36] عدم وجود فرق في عدد أيام الصداع النصفي، أو أيام الصداع، أو شدة الصداع، أو أيام استخدام التريبتانات. وتُعدّ الدراسات الحالية التي تقارن حبوب ديسوجيستريل الصغيرة بحبوب منع الحمل الفموية المركبة محدودة. ولا تسمح نتائج الدراسات الرصدية باستخلاص استنتاجات قاطعة بشأن الفعالية.
حبوب منع الحمل المركبة ذات الفترة الخالية من الحبوب القصيرة
فيما يخص استخدام موانع الحمل الفموية المركبة ذات الفترة الفاصلة القصيرة بين تناول الحبوب، لا تتوفر سوى دراسات ذات جودة منخفضة [4، 32]. وتُظهر هذه الدراسات أنظمة علاجية شديدة التباين. ولا يوجد دليل على تفوق أي نظام علاجي محدد مقارنةً بالخيارات الأخرى. كما أن الأدلة غير كافية لتبرير استخدام هذا العلاج حصراً للوقاية من الصداع النصفي. وقد اضطرت بعض النساء إلى إيقاف العلاج قبل الأوان بسبب تفاقم الصداع النصفي لديهن.
استخدام موانع الحمل الفموية المركبة مع تناول هرمون الإستروجين عن طريق الفم خلال "فترة التوقف عن تناول الحبوب"
لا تتوفر أدلة على استخدام موانع الحمل الهرمونية المركبة عن طريق الفم مع العلاج التعويضي بالإستروجين عن طريق الفم خلال فترة انقطاع تناول الحبوب إلا من دراسة واحدة فقط [39]. ولا تسمح البيانات الحالية بالتوصل إلى أي استنتاجات بشأن فعالية هذا النظام العلاجي في مسار الصداع النصفي.
استخدام موانع الحمل الفموية المركبة مع مكملات الإستراديول عبر لصقة خلال فترة الراحة من تناول الحبوب
في دراسة أجريت في مركز واحد، لم يُلاحظ أي انخفاض ملحوظ في عدد أيام الصداع النصفي، أو شدته، أو أعراضه [40]. وشملت الآثار الجانبية المرتبطة باستخدام الإستراديول عبر الجلد تغيرات في نزيف الانسحاب. ولا تُقدم البيانات الحالية مبرراً كافياً لاستخدام لصقات الإستراديول للوقاية من الصداع النصفي خلال فترة انقطاع تناول حبوب منع الحمل.
لصقات منع الحمل الهرمونية المركبة
البيانات المتعلقة باستخدام لصقات منع الحمل الهرمونية المركبة محدودة للغاية، إذ لا تتوفر سوى بيانات من دراسة واحدة [41]. تشير نتائج هذه الدراسة إلى وجود صلة بين انخفاض مستوى الهرمونات وحدوث الصداع، حيث كان عدد أيام الصداع أعلى خلال الأسبوع الذي لم تُستخدم فيه اللصقة. وبعد إزالة اللصقة عقب فترة علاج مطولة، لم يزد معدل تكرار الصداع. وبالتالي، لا تُقدم الأبحاث الحالية أدلة كافية تدعم استخدام هذا النهج.
حلقة مهبلية هرمونية مركبة لمنع الحمل
يُعدّ استخدام وسائل منع الحمل الهرمونية المركبة مع الحلقة المهبلية لعلاج الصداع النصفي محدودًا للغاية [42]. ولا تكفي البيانات المتاحة لتبرير استخدامها للوقاية من الصداع النصفي [4، 32].
مكملات الإستراديول عبر الجلد مع الجل
تمّ التحقق من تأثير استخدام جل الإستراديول عبر الجلد لدى النساء في سن ما قبل انقطاع الطمث في ثلاث دراسات [43-45]. أُعطي جل الإستراديول بجرعة 1.5 ملغ لمدة 6 أو 7 أيام، وقورن تأثيره بالدواء الوهمي. كان العلاج في هذه الدراسات مخصصًا للوقاية من الصداع. لم تُسجّل أيّة آثار جانبية خطيرة مرتبطة باستخدام جل الإستراديول. وُثّقت بعض الآثار الجانبية كالطفح الجلدي والقلق وانقطاع الطمث. وبناءً على الأدلة الحالية، فإنّ استخدام جل الإستراديول عبر الجلد للوقاية من الصداع النصفي غير مُبرّر بشكل كافٍ. فمن جهة، يُعدّ استخدام جل الإستراديول عبر الجلد بسيطًا وجيد التحمّل بشكل عام. ومن جهة أخرى، قد يُشكّل توقيت الاستخدام مشكلة في حالات عدم انتظام الدورة الشهرية. كما يُمكن أن يُشكّل احتمال زيادة أعراض الصداع النصفي نتيجةً لتأخر انخفاض مستوى الإستروجين عيبًا آخر. قد ينتج هذا عن زيادة جرعة الإستراديول مع تناول مكملات إضافية منه، وانخفاض ملحوظ في مستواه. كما يُمكن أن يُثبّط تناول الإستروجين الخارجي ارتفاع مستوى الإستروجين الداخلي في الجريبات. نظراً لقلة البيانات، لا يُنصح حالياً باستخدام جل الإستروجين للوقاية من الصداع النصفي المرتبط بالدورة الشهرية. ولا يُمكن اللجوء إلى هذا الأسلوب إلا في حال عدم فعالية جميع الاستراتيجيات الأخرى في الوقاية من هذا النوع من الصداع.
مكملات الإستراديول عبر الجلد عن طريق اللاصقة
الأدلة على استخدام لصقات الإستراديول عبر الجلد لعلاج الصداع النصفي المرتبط بالدورة الشهرية محدودة. ويكمن الأساس المنطقي لاستخدامها في الحفاظ على مستويات الإستراديول مستقرة قبل بدء الحيض [41]. حاليًا، لا توجد بيانات تُثبت فعالية لصقات الإستراديول في علاج الصداع النصفي.
مكملات الإستروجين عبر الجلد باستخدام اللصقات لدى النساء المصابات بانقطاع الطمث الناجم عن الأدوية
لا تُبرر البيانات الحالية استخدام لصقات الإستراديول عبر الجلد لدى النساء اللواتي يعانين من انقطاع الطمث المُستحث دوائيًا. خلال هذه المرحلة، يزداد خطر الإصابة بهشاشة العظام، والاكتئاب، والهبات الساخنة، والتهيج، وانخفاض الرغبة الجنسية، وجفاف المهبل. ويمكن تقليل هذا الخطر عن طريق العلاج التكميلي بالإستروجين [46]. ولا تكفي الأدلة الحالية لدعم استخدامها للوقاية من الصداع النصفي.
غرسة إستروجين تحت الجلد مع بروجستيرون دوري
أجرت دراسة رصدية مفتوحة التسمية بحثًا حول استخدام غرسة الإستروجين تحت الجلد مع البروجستوجين الدوري [47]. ولا تسمح البيانات المتاحة باستخلاص استنتاجات كافية بشأن استخدامها المحتمل في الوقاية من الصداع النصفي.
العلاج التعويضي
تمت دراسة مسار الصداع لدى النساء اللواتي يتناولن نظيرًا لهرمون إطلاق موجهة الغدد التناسلية (GnRH)، وهو محفز لانقطاع الطمث المؤقت الناتج عن العلاج، بالإضافة إلى لصقة إستروجين عبر الجلد، إما بمفردها أو بالاشتراك مع البروجستيرون (العلاج التعويضي) [48]. لوحظ انخفاض في شدة الصداع، ولكن ليس في تكراره. تشير هذه الدراسة إلى أن تقليل التقلبات الهرمونية قد يكون مفيدًا في الوقاية من الصداع النصفي خارج فترة الحيض.
الإستروجينات النباتية
الإستروجينات النباتية هي مركبات نباتية ثانوية مثل الإيسوفلافونات والليغنانات. وهي ليست إستروجينات بالمعنى الكيميائي، ولكنها تشترك معها في بعض الخصائص التركيبية. ينتج عن ذلك تأثير إستروجيني أو مضاد للإستروجين ضعيف. من أشهر الإستروجينات النباتية الإيسوفلافونات: الجينيستين، والدايدزين، والكوميسترول. يُستخدم الجينيستين والدايدزين، على وجه الخصوص، لتخفيف الهبات الساخنة وأعراض انقطاع الطمث الأخرى، بالإضافة إلى الصداع النصفي المرتبط بالدورة الشهرية. في دراسة مفتوحة التسمية استمرت 10 أيام خلال الدورة الشهرية (من -7 إلى +3 أيام)، لوحظ انخفاض متوسط في أيام الصداع بنسبة 62% [49]. أفاد نصف المرضى بعدم وجود غثيان أو قيء مصاحب للصداع النصفي. أكدت تجربة عشوائية مضبوطة هذا التأثير على مدى 24 أسبوعًا باستخدام نظام علاجي يتكون من 60 ملغ من إيسوفلافونات الصويا، و100 ملغ من دونغ كواي، و50 ملغ من الكوهوش الأسود [50]. أظهرت هذه الدراسة انخفاضًا ملحوظًا في الصداع النصفي المرتبط بالدورة الشهرية، واستخدام الأدوية المسكنة، وشدة الصداع. لذا، قد تُشكل الإستروجينات النباتية خيارًا مناسبًا للنساء اللواتي لا يرغبن في تناول العلاجات الهرمونية أو لا يستطعن استخدامها بسبب موانع الاستخدام، مثل ارتفاع خطر الإصابة بأمراض القلب والأوعية الدموية.
علاجات هرمونية إضافية
أظهرت الدراسات التي تناولت استخدام وسائل منع الحمل للوقاية من الصداع أن تحفيز انقطاع الطمث يرتبط بانخفاض ملحوظ في نوبات الصداع [4، 32]. وتتميز العلاجات التي تعتمد على البروجسترون فقط بانخفاض خطر الإصابة بأمراض القلب والأوعية الدموية أو مضاعفاتها مقارنةً بالإستروجينات [4، 30، 33]. كما يمكن أن تكون هذه العلاجات فعالة في الوقاية من الصداع النصفي المصحوب بهالة. وبفضل الاستخدام المستمر، لا تحدث تقلبات هرمونات الأنوثة المرتبطة بالدورة الشهرية ولا أعراض الانسحاب الحاد للإستروجين.
أظهرت الدراسات قبل السريرية أن هرمون التستوستيرون يثبط الاكتئاب القشري المنتشر [51]. ويمكن أن يقلل الحقن تحت الجلد لغرسات التستوستيرون من شدة الصداع لدى المرضى الذين يعانون من قصور الأندروجين. وبعد استئصال المبيضين المصحوب بقصور الأندروجين، أبلغت النساء عن زيادة في وتيرة الصداع النصفي مقارنةً بالنساء اللواتي يدخلن سن اليأس الطبيعي [52].
غالباً ما تعاني النساء اللواتي يخضعن للعلاج الهرموني التعويضي خلال فترة انقطاع الطمث من تفاقم الصداع [53]. ويرجع ذلك على الأرجح إلى عدم انتظام إفراز هرمون الإستروجين. وقد يساعد العلاج الهرموني التعويضي في استقرار انخفاض مستوى الإستروجين في هذه الحالة. ينبغي استخدام أقل جرعة فعالة للسيطرة على أعراض انقطاع الطمث وتجنب الآثار الجانبية القلبية الوعائية، لا سيما في حالات الصداع النصفي المصحوب بهالة. وقد يكون استخدام الإستروجين عبر الجلد أو اتباع أنظمة علاجية مركبة مستمرة، مثل العلاج الهرموني التعويضي، والتي تمنع النزيف، هو الأسلوب الأمثل للوقاية من الصداع النصفي في هذه الحالة.
توبيراميت، والصداع النصفي المرتبط بالدورة الشهرية، ومنع الحمل
تمت الموافقة على استخدام توبيراميت كعلاج وقائي للصداع النصفي، كما يُستخدم لعلاج الصداع النصفي المرتبط بالدورة الشهرية. عند استخدام جرعات يومية من توبيراميت تزيد عن 200 ملغ، ينبغي مراعاة احتمال انخفاض فعالية منع الحمل وزيادة النزيف غير المنتظم لدى النساء اللواتي يستخدمن حبوب منع الحمل المركبة [54]. يجب نصح النساء اللواتي يستخدمن موانع الحمل المحتوية على الإستروجين بإبلاغ مقدم الرعاية الصحية بأي تغييرات في الدورة الشهرية. قد تنخفض فعالية منع الحمل مع استخدام توبيراميت حتى في حال عدم وجود نزيف غير منتظم [55].
CGRP-mAK والصداع النصفي المرتبط بالحيض
لا يوجد حاليًا علاج وقائي محدد للصداع النصفي المرتبط بالدورة الشهرية. وقد دُرست مؤخرًا إمكانية استخدام الأجسام المضادة وحيدة النسيلة ضد الببتيد المرتبط بجين الكالسيتونين (CGRP) أو مستقبلاته لعلاج هذا النوع من الصداع. ونظرًا لطول عمر النصف لهذه الأجسام المضادة، فإنها تتميز، خاصةً في العلاج طويل الأمد، بأنها لا تحتاج إلا إلى تناولها شهريًا أو كل ثلاثة أشهر. وتتوفر الآن في ألمانيا أدوية غالكانزوماب، وإيرينوماب، وإيبتينيزوماب، وفريمانيزوماب كعلاج وقائي للصداع النصفي. في دراسة أجريت على إيرينوماب [56]، قورن مسار الصداع النصفي المرتبط بالدورة الشهرية بين مجموعتين: مجموعة استجابت للعلاج ومجموعة لم تستجب له. وأظهرت النتائج أن وتيرة الصداع كانت أعلى خلال فترة الحيض مقارنةً بغيرها في كلتا المجموعتين. وهذا يعني أنه حتى مع العلاج بإيرينوماب، فإن الصداع النصفي يحدث بوتيرة أكبر خلال فترة الحيض مقارنةً بغيرها. وفي دراسة أخرى، تم تحليل فعالية إيرينوماب في الوقاية من الصداع النصفي المرتبط بالدورة الشهرية [57]. شملت أيام الصداع النصفي الشهرية نوبات الصداع النصفي المصاحبة للدورة الشهرية والنوبات بين الدورات الشهرية. وقد أدى استخدام إيرينوماب بجرعتي 70 ملغ و140 ملغ إلى انخفاض ملحوظ في عدد أيام الصداع النصفي شهريًا مقارنةً بالدواء الوهمي. وتُظهر هذه البيانات فعالية إيرينوماب في الوقاية من الصداع النصفي المرتبط بالدورة الشهرية [57].
مخاطر الإصابة بأمراض القلب والأوعية الدموية
يُعاني مرضى الشقيقة من خطر الإصابة بالسكتة الدماغية بمقدار الضعف تقريبًا مقارنةً بالأصحاء. وينطبق هذا بشكل خاص على الشقيقة المصحوبة بهالة. تُعدّ الشقيقة عامل خطر للإصابة بالسكتة الدماغية، لا يقل أهمية عن عوامل أخرى مثل فرط التخثر، والثقبة البيضوية المفتوحة، وتسلخ الشريان، والتدخين، والسمنة [4، 30، 32، 33، 58-60].
تُحسّن هرمونات الإستروجين تدفق الدم المعتمد على البطانة الوعائية ومستويات الدهون في الدم. مع ذلك، لها أيضًا تأثيرات مُحفّزة للتخثر والالتهاب. قد تكون هذه التأثيرات ذات أهمية خاصة لدى المرضى المعرضين لخطر متزايد للإصابة بالسكتة الدماغية وغيرها من الأحداث الوعائية مثل احتشاء عضلة القلب أو تجلط الأوردة العميقة. قد يرتبط استخدام موانع الحمل الفموية المركبة بظهور السكتة الدماغية في سن مبكرة [4، 32، 61، 62].
من حيث المبدأ، يجب دراسة وجود عاملين مستقلين من عوامل خطر الإصابة بالسكتة الدماغية بعناية. تشير الدراسات إلى أن النساء المصابات بالصداع النصفي واللاتي يستخدمن أيضًا موانع الحمل الهرمونية المركبة لديهن خطر متزايد للإصابة بالسكتة الدماغية بنسبة تتراوح بين 2.1 و13.9 [33، 61]. يرتبط خطر الإصابة بالسكتة الدماغية بجرعة الإستروجين. لذلك، لا توصي الإرشادات الصادرة عن الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH) [32، 33]، والجمعية الألمانية لطب الأعصاب (DGN) بالتعاون مع الجمعية الألمانية للصداع النصفي والصداع [63]، والجمعية الألمانية لأمراض النساء والتوليد [62] باستخدام موانع الحمل الهرمونية المركبة للمريضات المصابات بالصداع النصفي المصحوب بهالة. أما المريضات المصابات بالصداع النصفي غير المصحوب بهالة، فلا ينبغي لهن استخدام موانع الحمل الهرمونية المركبة في حال وجود عوامل خطر وعائية أخرى. بدلاً من ذلك، يمكن النظر في وسائل منع الحمل التي تحتوي على البروجستوجين فقط أو وسائل منع الحمل الفموية المركبة بجرعات من الإستروجين أقل من 35 ميكروغرام.
للوقاية من الصداع النصفي المرتبط بالدورة الشهرية، يمكن استخدام أنظمة علاجية ذات دورات شهرية ممتدة وعلاجات تحافظ على استقرار مستويات الهرمونات، مثل الحقن المهبلي أو مكملات الإستراديول عبر الجلد. كما يمكن النظر في استخدام جرعات منخفضة من الإستروجين لهؤلاء المريضات. مع ذلك، لا تزال البيانات الحالية غير كافية لإصدار أحكام موثوقة حول فعالية هذه العلاجات ومدى تحملها. على الرغم من أن العلاج الأحادي بالبروجستين يتميز بأقل مخاطر على الأوعية الدموية، إلا أنه قد تحدث آثار جانبية مثل النزيف غير المنتظم.
بشكل عام، تُظهر الدراسات أن العلاج بالإستروجين هو العلاج الأكثر فعالية والأفضل تحملاً. وستكون الدراسات المستقبلية حول فعالية الإستروجين الطبيعي ومدى تحمله مهمة أيضاً. ومن المرجح أن تكون فترة انقطاع قصيرة عن الهرمونات هي الطريقة الأكثر فعالية لمنع انخفاض مستويات الإستروجين الذي قد يُحفز نوبة الصداع النصفي. ومع ذلك، هناك حاجة إلى مزيد من الدراسات المضبوطة للتوصل إلى استنتاجات موثوقة في هذا المجال.
التوصيات الإرشادية الحالية للوقاية من الصداع النصفي المرتبط بالدورة الشهرية
توصي الإرشادات الحالية الصادرة عن الجمعية الألمانية لطب الأعصاب (DGN) بالتعاون مع الجمعية الألمانية للصداع النصفي والصداع [63] لعام 2022 باستخدام النابروكسين، وهو مضاد التهاب غير ستيرويدي طويل المفعول (نصف عمره 12-15 ساعة)، أو أحد التريبتانات طويلة المفعول للوقاية قصيرة الأمد من الصداع النصفي المرتبط بالدورة الشهرية. يجب تناول هذه الأدوية لمدة 5-6 أيام، بدءًا من يومين قبل الموعد المتوقع لبدء الدورة الشهرية. كما يمكن النظر في الاستخدام المستمر لحبوب منع الحمل المركبة كإجراء وقائي. ويمكن أيضًا النظر في استخدام ديسوجيستريل للوقاية من الصداع النصفي المرتبط بالدورة الشهرية.
توجد دراسات مضبوطة بالغفل لاستخدام فروفاتريبتان بجرعة 2.5 ملغ مرة أو مرتين أو ثلاث مرات يوميًا، وزولميتريبتان بجرعة 2.5 ملغ مرتين أو ثلاث مرات يوميًا، وناراتريبتان بجرعة 1 ملغ أو 2.5 ملغ مرتين يوميًا، ونابروكسين بجرعة 550 ملغ مرتين يوميًا. يجب أن يبدأ تناول هذه الأدوية قبل يومين من الموعد المتوقع لبدء نوبة الصداع النصفي خلال فترة الحيض، ويستمر لمدة 6-7 أيام. يُعتبر خطر الإصابة بصداع ناتج عن الإفراط في استخدام الأدوية عند استخدام نابروكسين أو أحد التريبتانات للوقاية قصيرة الأمد من الصداع النصفي المرتبط بالحيض منخفضًا، شريطة عدم استخدام أدوية أخرى كثيرة لعلاج النوبات الحادة.
لا توصي الإرشادات الحالية بإعطاء الإستروجين عن طريق الجلد، وذلك بسبب تأخر ظهور نوبات الصداع النصفي بعد التوقف عن استخدام جل الإستروجين. ولا يُنصح بتناول الإستروجين عن طريق الجلد إلا في حال عدم فعالية التدابير الوقائية الأخرى. ومن الشروط الأساسية لهذا النهج انتظام الدورة الشهرية لتحديد التوقيت الأمثل للاستخدام. كما لا يُنصح بتناول الإستروجين عن طريق الجلد خلال فترة انقطاع حبوب منع الحمل للوقاية من الصداع النصفي المرتبط بالدورة الشهرية، وذلك لعدم توفر بيانات كافية.
وفقًا للإرشادات الحالية، يُمكن اعتبار الاستخدام المستمر لحبوب منع الحمل المركبة إجراءً وقائيًا. والهدف هو تقليل عدد دورات الحيض ونوبات الصداع النصفي التي تُسببها. ويُعتبر الاستخدام المستمر لمدة تصل إلى عامين آمنًا. تُشير الإرشادات إلى أن هذا العلاج الوقائي للصداع ونوبات الصداع النصفي خارج فترة الحيض لم يُدرس حتى الآن إلا في دراسات مفتوحة وغير مضبوطة. ونظرًا لأن حبوب منع الحمل المركبة قد تزيد بشكل ملحوظ من خطر الإصابة بالسكتة الدماغية، ولأن الصداع النصفي المصحوب بهالة يُعدّ بحد ذاته عامل خطر للإصابة بالسكتة الدماغية، فيجب مراعاة عوامل الخطر القلبية الوعائية لكل مريضة على حدة. ووفقًا للإرشادات، يُعدّ الاستخدام المستمر لحبوب منع الحمل المركبة أقل إشكالية لدى المريضات المصابات بالصداع النصفي غير المصحوب بهالة واللاتي لا يُعانين من عوامل خطر قلبية وعائية أخرى. وفيما عدا ذلك، يجب تحديد دواعي الاستخدام بدقة، وإبلاغ المريضات بشكل كافٍ، واتخاذ القرار بشأن الإجراء بناءً على كل حالة على حدة. ويُفضّل عمومًا استخدام حبوب منع الحمل المركبة ذات المحتوى المنخفض من الإستروجين. يُعد الصداع النصفي النشط للغاية المصحوب بهالة لدى المرضى الذين لديهم عوامل خطر وعائية مرتفعة أحد موانع استخدام موانع الحمل الفموية المركبة.
يجب أيضاً ضمان استخدام وسائل منع الحمل المناسبة أثناء مختلف العلاجات الوقائية للصداع النصفي. وينطبق هذا بشكل خاص على العلاج بالأجسام المضادة وحيدة النسيلة ضد الببتيد المرتبط بجين الكالسيتونين (CGRP) أو مستقبل CGRP، وسم البوتولينوم، والفلواريزين، والتوبيراميت، والفالبروات.
موانع الحمل الهرمونية، خطر الإصابة بالسكتة الدماغية والصداع النصفي في الممارسة العملية
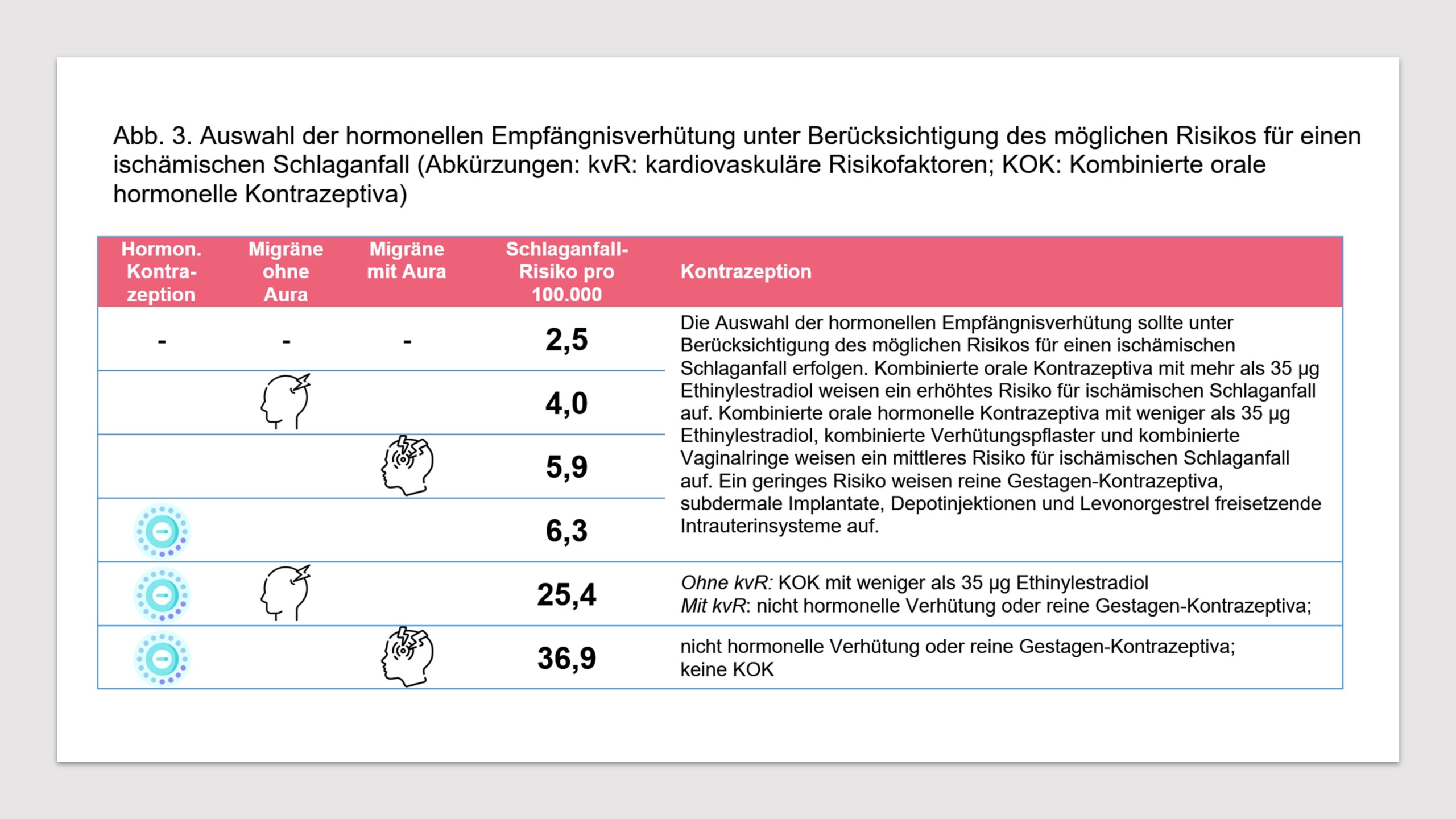
يُعدّ الصداع النصفي عامل خطر للإصابة بالسكتة الدماغية وغيرها من الأحداث الوعائية. وتوجد أدلة كثيرة تشير إلى أن زيادة خطر الإصابة بالسكتة الدماغية الإقفارية يرتبط بكلٍ من الصداع النصفي بدون هالة والصداع النصفي مع هالة [4، 30، 32، 33، 58-60]. ونظرًا لأن خطر الإصابة بالسكتة الدماغية قد يزداد أيضًا مع استخدام موانع الحمل الهرمونية المركبة [4، 32، 61]، يثور التساؤل عما إذا كان التزامن بين الصداع النصفي واستخدام موانع الحمل الهرمونية المركبة يزيد من خطر الإصابة بالسكتة الدماغية. وقد قام الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH) بتحليل هذا التساؤل في بيان توافقي [33]. ويبلغ الخطر المطلق للإصابة بالسكتة الدماغية الإقفارية لدى النساء اللاتي لا يستخدمن موانع الحمل الهرمونية 2.5 لكل 100,000 امرأة سنويًا. بينما يبلغ الخطر نفسه 6.3 لكل 100,000 امرأة لدى النساء اللاتي يستخدمن موانع الحمل الهرمونية. بالنسبة للنساء المصابات بالصداع النصفي المصحوب بهالة، يبلغ خطر الإصابة بسكتة دماغية إقفارية دون استخدام موانع الحمل الهرمونية 5.9 لكل 100,000 امرأة سنويًا. أما خطر الإصابة بسكتة دماغية إقفارية مع الصداع النصفي المصحوب بهالة واستخدام موانع الحمل الهرمونية فيبلغ 36.9 لكل 100,000 امرأة سنويًا. وبالنسبة للنساء المصابات بالصداع النصفي غير المصحوب بهالة، يبلغ خطر الإصابة بسكتة دماغية إقفارية 4.0 لكل 100,000 امرأة سنويًا. وفي حال استخدام موانع الحمل الهرمونية في هذه المجموعة، يرتفع الخطر إلى 25.4 لكل 100,000 امرأة سنويًا (انظر الشكل 3).
استنادًا إلى البيانات، توصل الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH) إلى توافق آراء الخبراء التالي [33]:
- إذا كانت النساء يرغبن في استخدام وسائل منع الحمل الهرمونية، يُنصح بإجراء فحص سريري لتحديد ما إذا كنّ يعانين من الصداع النصفي المصحوب بهالة أو غير المصحوب بها. بالإضافة إلى ذلك، ينبغي تقييم عدد نوبات الصداع النصفي (عدد أيام الصداع شهريًا) وتحديد عوامل الخطر الوعائية قبل وصف وسائل منع الحمل الهرمونية المركبة.
- يُنصح النساء الراغبات في استخدام وسائل منع الحمل الهرمونية باستخدام أداة خاصة لتشخيص الصداع النصفي وأنواعه الفرعية. قد تشمل هذه الأداة استبيانات أو خيارات رقمية مثل تطبيق الصداع النصفي (المتوفر للتنزيل مجانًا بهذا الاسم في متاجر التطبيقات).
- ينبغي اختيار وسيلة منع الحمل الهرمونية مع مراعاة احتمالية الإصابة بالسكتة الدماغية الإقفارية. تزيد حبوب منع الحمل المركبة التي تحتوي على أكثر من 35 ميكروغرام من الإيثينيل إستراديول من خطر الإصابة بالسكتة الدماغية الإقفارية. أما حبوب منع الحمل الهرمونية المركبة التي تحتوي على أقل من 35 ميكروغرام من الإيثينيل إستراديول، واللصقات المهبلية المركبة، والحلقات المهبلية المركبة، فتُشكل خطرًا متوسطًا للإصابة بالسكتة الدماغية الإقفارية. بينما تُشكل وسائل منع الحمل التي تحتوي على البروجستيرون فقط، والغرسات تحت الجلد، والحقن طويلة المفعول، واللولب الرحمي المُطلق لليفونورجيستريل، خطرًا منخفضًا.
- يُنصح النساء اللواتي يعانين من الصداع النصفي المصحوب بهالة واللواتي يرغبن في استخدام وسائل منع الحمل الهرمونية بعدم وصف وسائل منع الحمل الهرمونية المركبة لهن.
- يُنصح النساء المصابات بالصداع النصفي المصحوب بهالة والراغبات في استخدام وسائل منع الحمل، باستخدام الوسائل غير الهرمونية (الواقي الذكري، أو اللولب النحاسي، أو موانع الحمل التي تحتوي على البروجستين فقط) كخيار مفضل. في حال وجود الصداع النصفي المصحوب بهالة واستخدام موانع الحمل الهرمونية المركبة، يُنصح بالتحول إلى موانع الحمل غير الهرمونية أو موانع الحمل التي تحتوي على البروجستين فقط.
- بالنسبة للنساء اللواتي يعانين من الصداع النصفي بدون هالة واللواتي يرغبن في استخدام وسائل منع الحمل الهرمونية ولكن لديهن عوامل خطر إضافية (التدخين، ارتفاع ضغط الدم الشرياني، السمنة، أمراض القلب والأوعية الدموية، تجلط الأوردة العميقة أو الانسداد الرئوي في الماضي)، يوصى باستخدام وسائل منع الحمل غير الهرمونية أو وسائل منع الحمل التي تحتوي على البروجستيرون فقط كخيار مفضل.
- بالنسبة للنساء المصابات بالصداع النصفي بدون هالة واللاتي يستخدمن موانع الحمل الهرمونية وليس لديهن عوامل خطر إضافية، يُنصح باستخدام موانع الحمل الهرمونية المركبة بجرعة أقل من 35 ميكروغرام من الإيثينيل إستراديول كوسيلة لمنع الحمل. ويجب في الوقت نفسه مراقبة تواتر الصداع النصفي وخصائصه.
- إذا كانت النساء يعانين من الصداع النصفي المصحوب بهالة أو الصداع النصفي غير المصحوب بهالة ويحتجن إلى علاج هرموني بسبب متلازمة تكيس المبايض أو الانتباذ البطاني الرحمي، فمن المستحسن استخدام العلاج الهرموني بالبروجستينات فقط أو موانع الحمل الهرمونية المركبة وفقًا للاعتبارات السريرية.
- إذا أصيبت النساء اللواتي بدأن باستخدام وسائل منع الحمل الهرمونية المركبة بصداع نصفي جديد مصحوب بهالة، أو اللواتي يعانين من الصداع النصفي بدون هالة لأول مرة في علاقة زمنية وثيقة ببدء استخدام وسائل منع الحمل الهرمونية، يُنصح بالتحول إلى وسائل منع الحمل غير الهرمونية أو وسائل منع الحمل التي تحتوي على البروجستيرون فقط.
- إذا كانت النساء اللواتي يعانين من الصداع النصفي مع أو بدون هالة يحتجن إلى وسائل منع الحمل الطارئة، يوصى باستخدام ليفونورجيستريل 1.5 ملغ عن طريق الفم، أو أسيتات أوليبريستال 30 ملغ عن طريق الفم، أو جهاز داخل الرحم يحتوي على النحاس.
- إذا بدأت النساء المصابات بالصداع النصفي مع أو بدون هالة في استخدام وسائل منع الحمل الهرمونية، فإن الاختبارات المحددة مثل فحص التخثر الدموي، أو فحص الثقبة البيضوية المفتوحة، أو إجراءات التصوير ليست ذات صلة بالقرار المتعلق بوسائل منع الحمل الهرمونية، إلا إذا كان التاريخ الطبي أو النتائج تتطلب مثل هذه التحقيقات بناءً على مؤشرات محددة.
- يمكن استخدام أي وسيلة منع حمل هرمونية منخفضة الجرعة لدى النساء المصابات بالصداع غير النصفي واللواتي يرغبن في استخدام وسائل منع الحمل الهرمونية.
بشكل عام، الأدلة المتعلقة بالصلة بين السكتة الدماغية الإقفارية واستخدام موانع الحمل الهرمونية محدودة. في الواقع، لا توجد سوى دراسات رصدية غير مضبوطة. هناك حاجة إلى مزيد من الدراسات لتحديد المخاطر المحتملة لموانع الحمل الهرمونية لدى النساء المصابات بالصداع النصفي بدقة أكبر. ومع ذلك، تشير البيانات الحالية إلى زيادة خطر الإصابة بالسكتة الدماغية الإقفارية المرتبطة باستخدام موانع الحمل الهرمونية لدى النساء المصابات بالصداع النصفي. في هذه الحالة، من الضروري إيلاء اهتمام خاص لجوانب السلامة أثناء الاستخدام. حتى لو لم يكن الخطر المطلق للإصابة بالسكتة الدماغية مرتفعًا جدًا، فقد تكون لها عواقب وخيمة على الأفراد وعائلاتهم. لهذه الأسباب، ينبغي النظر في وسائل منع الحمل البديلة عند وجود زيادة مماثلة في الخطر.
الأدب
- لجنة تصنيف الصداع التابعة للجمعية الدولية للصداع (IHS)، التصنيف الدولي لاضطرابات الصداع ICHD-3، الطبعة الثالثة. مجلة سيفالجيا، 2018. 38 (1): ص 1-211.
- تصنيف ومعايير تشخيص اضطرابات الصداع، وآلام الأعصاب القحفية، وآلام الوجه. لجنة تصنيف الصداع التابعة للجمعية الدولية للصداع. مجلة سيفالجيا، 1988. 8 ملحق 7 : ص 1-96.
- التصنيف الدولي لاضطرابات الصداع: الطبعة الثانية. مجلة سيفالجيا، 2004. 24 ملحق 1 : ص 9-160.
- نابي، آر إي، وآخرون، دور الإستروجينات في الصداع النصفي المرتبط بالحيض. الخلايا، 2022. 11 (8).
- راسل، إم بي، علم الوراثة للصداع النصفي المرتبط بالحيض: الأدلة الوبائية. تقارير الألم والصداع الحالية، 2010. 14 (5): ص 385-8.
- سومرفيل، بي دبليو، دور انسحاب الإستراديول في مسببات الصداع النصفي المرتبط بالحيض. علم الأعصاب، 1972. 22 (4): ص. 355-65.
- بافلوفيتش، جيه إم، وآخرون، الهرمونات الجنسية لدى النساء المصابات وغير المصابات بالصداع النصفي. علم الأعصاب، 2016. 87 (1): ص 49.
- كورنيل، سي إيه، جي إف بول، وجيه بالتزارت، الأهمية الوظيفية للتنظيم السريع لعمل هرمون الاستروجين في الدماغ: من أين تأتي هرمونات الاستروجين؟ أبحاث الدماغ، 2006. 1126 (1): ص. 2-26.
- بوز، أ.س.، وآخرون، الاختلافات الجنسية في وظائف الأوعية الدموية ومرضها: إشارات الإستروجين والأندروجين في الصحة والمرض. المجلة الأمريكية لعلم وظائف الأعضاء - القلب والدورة الدموية، 2017. 313 (3): ص. H524-H545.
- رودريغيز-أسيفيدو، إيه جيه، وآخرون، تشير دراسات الارتباط الجيني والتعبير الجيني إلى أن المتغيرات الجينية في جيني SYNE1 وTNF مرتبطة بالصداع النصفي المرتبط بالحيض. مجلة الصداع والألم، 2014. 15 (1): ص 62.
- فيتفيك، كيه جي وماكجريجور، إي إيه، الصداع النصفي المرتبط بالحيض: اضطراب متميز يحتاج إلى مزيد من الاعتراف. مجلة لانسيت لعلم الأعصاب، 2021. 20 (4): ص 304-315.
- شوغرو، بي جيه، وميرشنثالر، آي.، الإستروجين ليس مجرد "هرمون جنسي": مواقع جديدة لعمل الإستروجين في الحصين والقشرة المخية. فرونت نيوروإندوكرينول، 2000. 21 (1): ص 95-101.
- فاكينيتي، ف.، وآخرون، التقييم العصبي الصماوي لنشاط الأفيون المركزي في اضطرابات الصداع الأولية. الألم، 1988. 34 (1): ص. 29-33.
- تاسوريلي، سي، وآخرون، تغيرات في عتبة منعكس الانثناء المؤلم خلال الدورة الشهرية لدى النساء الأصحاء. الطب النفسي الجسدي، 2002. 64 (4): ص. 621-6.
- كراوس، دي إن، وآخرون، التأثيرات الهرمونية في الشقيقة - تفاعلات الإستروجين والأوكسيتوسين وCGRP. نات ريف نيورول، 2021. 17 (10): ص. 621-633.
- دي إيكو، ر.، وآخرون، تعديل عتبة الألم بواسطة موانع الحمل الهرمونية المركبة لدى النساء المصابات بنوبات الصداع النصفي الناتجة عن انخفاض هرمون الإستروجين: دراسة تجريبية. مجلة الصداع والألم، 2016. 17 (1): ص. 70.
- وارفينج، ك.، وآخرون، مستقبلات الإستروجين α و β و GPER في الجهاز العصبي المركزي والجهاز الثلاثي التوائم - الجوانب الجزيئية والوظيفية. مجلة الصداع والألم، 2020. 21 (1): ص 131.
- كيتازاوا، ت.، وآخرون، الآلية غير الجينومية لتثبيط الانقباض الناجم عن هرمون الإستراديول-17 بيتا في العضلات الملساء الوعائية لدى الثدييات. مجلة علم وظائف الأعضاء، 1997. 499 (الجزء 2 ): ص 497-511.
- سومجين، جي جي، آليات الاكتئاب المنتشر والاستقطاب المشابه للاكتئاب المنتشر الناتج عن نقص الأكسجين. مجلة علم وظائف الأعضاء، 2001. 81 (3): ص. 1065-96.
- إدفينسون، ل.، وآخرون، CGRP كهدف لعلاجات جديدة للصداع النصفي - ترجمة ناجحة من المختبر إلى العيادة. نات ريف نيورول، 2018. 14 (6): ص. 338-350.
- ، الذي طوره كل من نايت، واي إي، وإدفينسون، وبي جيه غودسبي، إطلاق الببتيد المرتبط بجين الكالسيتونين في القطط، ولكن فقط عند الجرعات التي لها نشاط ناهض لمستقبلات 5HT(1B/1D)؟ علم الأدوية العصبية، 2001. 40 (4): ص. 520-5.
- أشينا، م.، الصداع النصفي. مجلة نيو إنجلاند الطبية، 2020. 383 (19): ص. 1866-1876.
- فوربس، آر بي، إم. ماكارون، وسي آر كاردويل، فعالية وتأثيرات سياقية (بلاسيبو) للأجسام المضادة لـ CGRP لعلاج الصداع النصفي: مراجعة منهجية وتحليل تجميعي. الصداع، 2020. 60 (8): ص. 1542-1557.
- دريليا، ك.، وآخرون، الأجسام المضادة وحيدة النسيلة المضادة لـ CGRP للوقاية من الصداع النصفي: مراجعة منهجية وتحليل احتمالية المساعدة أو الضرر. سيفالجيا، 2021. 41 (7): ص 851-864.
- فالديمارسون، إس.، وآخرون، التأثير الهرموني على الببتيد المرتبط بجين الكالسيتونين لدى الإنسان: تأثيرات الاختلافات الجنسية وحبوب منع الحمل. مجلة سكاندينافية للتحقيقات السريرية والمخبرية، 1990. 50 (4): ص 385-8.
- غوبتا، ب.، وآخرون، تأثير حالة انقطاع الطمث على الببتيد المرتبط بجين الكالسيتونين والأديبوكينات في الدورة الدموية: الآثار المترتبة على مقاومة الأنسولين ومخاطر القلب والأوعية الدموية. مجلة انقطاع الطمث، 2008. 11 (5): ص 364-72.
- أغاروال، م.، ف. بوري، وس. بوري، تأثيرات الإستروجين على نظام السيروتونين وببتيد الكالسيتونين المرتبط بالجين في العقد العصبية الثلاثية التوائم للفئران. حوليات علم الأعصاب، 2012. 19 (4): ص. 151-7.
- سيتينكايا، أ.، وآخرون، تأثيرات الإستروجين والبروجسترون على الببتيدات العصبية الالتهابية: دلالات على الاختلافات بين الجنسين في الصداع النصفي. مجلة أبحاث الدماغ التجريبية، 2020. 238 (11): ص. 2625-2639.
- ياماناكا، جي، وآخرون، دور الالتهاب العصبي وقابلية تبديل الحاجز الدموي الدماغي في الصداع النصفي. المجلة الدولية للعلوم الجزيئية، 2021. 22 (16).
- كوبيني، إل إم، آي. كوربيلي، وبي. سارتشيلي، الصداع النصفي المرتبط بالحيض: ما هو وهل هو مهم؟ مجلة علم الأعصاب، 2021. 268 (7): ص. 2355-2363.
- ماكجريجور، إي إيه، وآخرون، نسبة حدوث الصداع النصفي بالنسبة لمراحل الدورة الشهرية التي تشهد ارتفاعاً وانخفاضاً في هرمون الإستروجين. علم الأعصاب، 2006. 67 (12): ص. 2154-8.
- ساكو، إس.، وآخرون، تأثير الإستروجينات والبروجستوجينات الخارجية على مسار الصداع النصفي خلال سن الإنجاب: بيان توافقي صادر عن الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH). مجلة الصداع والألم، 2018. 19 (1): ص 76.
- ساكو، إس.، وآخرون، موانع الحمل الهرمونية وخطر الإصابة بالسكتة الدماغية الإقفارية لدى النساء المصابات بالصداع النصفي: بيان توافقي من الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESC). مجلة الصداع والألم، 2017. 18 (1): ص 108.
- ميركي-فيلد، جي إس، وآخرون، تحسن الصداع النصفي مع التحول من موانع الحمل الهرمونية المركبة إلى موانع الحمل التي تحتوي على البروجستين فقط مع ديسوجيستريل: ما مدى قوة تأثير إيقاف النساء عن استخدام موانع الحمل المركبة؟ مجلة طب التوليد وأمراض النساء، 2017. 37 (3): ص. 338-341.
- موروتي، م.، وآخرون، مقارنة حبوب منع الحمل التي تحتوي على البروجستيرون فقط مع حبوب منع الحمل المركبة في علاج أعراض الألم الناجمة عن الانتباذ البطاني الرحمي لدى المرضى المصابين بالصداع النصفي بدون هالة. المجلة الأوروبية لأمراض النساء والتوليد والبيولوجيا الإنجابية، 2014. 179 : ص 63-8.
- موروتي، م.، وآخرون، مقارنة وسائل منع الحمل التي تحتوي على البروجستين فقط مع وسائل منع الحمل الفموية المركبة الممتدة لدى النساء المصابات بالصداع النصفي بدون هالة: دراسة تجريبية استرجاعية. المجلة الأوروبية لأمراض النساء والتوليد والبيولوجيا الإنجابية، 2014. 183 : ص 178-182.
- نابي، ر. إي.، وآخرون، آثار مانع حمل فموي خالٍ من الإستروجين يحتوي على ديسوجيستريل لدى النساء المصابات بالصداع النصفي المصحوب بهالة: دراسة تجريبية مستقبلية قائمة على اليوميات. منع الحمل، 2011. 83 (3): ص 223-228.
- كوفي، أ.ل.، وآخرون، موانع الحمل الفموية المركبة ذات الدورة الممتدة مع استخدام فروفاتريبتان كوقاية خلال الفترة الخالية من الهرمونات لدى النساء المصابات بالصداع النصفي المرتبط بالحيض. مجلة صحة المرأة (لارشمونت)، 2014. 23 (4): ص 310-317.
- كالهون، أ.هـ.، وقاية نوعية جديدة للصداع النصفي المرتبط بالحيض. مجلة ساوث ميد، 2004. 97 (9): ص. 819-22.
- ماكجريجور، إي. أ. وهاكشو، أ.، الوقاية من الصداع النصفي خلال الفترة الخالية من حبوب منع الحمل المركبة: دراسة تجريبية مزدوجة التعمية مضبوطة بالغفل باستخدام مكملات الإستروجين الطبيعية. مجلة تنظيم الأسرة والرعاية الصحية الإنجابية، 2002. 28 (1): ص 27-31.
- لاغوارديا، ك.د.، وآخرون، تثبيط الصداع الناتج عن انسحاب الإستروجين باستخدام وسائل منع الحمل عبر الجلد لفترة طويلة. مجلة الخصوبة والعقم، 2005. 83 (6): ص. 1875-7.
- كالهون، أ.، إس. فورد، وأ. برويت، تأثير استخدام حلقة منع الحمل المهبلية ذات الدورة الممتدة على هالة الصداع النصفي: سلسلة حالات استرجاعية. الصداع، 2012. 52 (8): ص. 1246-53.
- de Lignières، B.، وآخرون، الوقاية من الصداع النصفي الحيضي عن طريق استراديول عن طريق الجلد. بر ميد جي (كلين ريس إد)، 1986. 293 (6561): ص. 1540.
- دينرستين، ل.، وآخرون، الصداع النصفي المرتبط بالحيض: تجربة مزدوجة التعمية للإستراديول عن طريق الجلد. أمراض النساء والغدد الصماء، 1988. 2 (2): ص. 113-20.
- ماكجريجور، إي إيه، وآخرون، الوقاية من نوبات الصداع النصفي المرتبطة بالحيض: دراسة مزدوجة التعمية مضبوطة بالغفل. علم الأعصاب، 2006. 67 (12): ص. 2159-63.
- مارتن، ف.، وآخرون، استئصال المبيض الطبي مع وبدون العلاج التعويضي بالإستروجين في الوقاية من الصداع النصفي. الصداع، 2003. 43 (4): ص. 309-21.
- ماجوس، أ.ل.، ك.ج. زيلخا، وج.و. ستاد، علاج الصداع النصفي المرتبط بالحيض باستخدام غرسات الإستراديول. مجلة علم الأعصاب وجراحة الأعصاب والطب النفسي، 1983. 46 (11): ص. 1044-6.
- موراي، إس سي، وكي إن ميوز، العلاج الفعال للصداع النصفي الشديد المصاحب للدورة الشهرية باستخدام ناهض هرمون إطلاق موجهة الغدد التناسلية والعلاج التعويضي. مجلة الخصوبة والعقم، 1997. 67 (2): ص 390-3.
- فيرانتي، ف.، وآخرون، الإستروجينات النباتية في الوقاية من الصداع النصفي المرتبط بالحيض. علم الأدوية العصبية السريرية، 2004. 27 (3): ص. 137-40.
- بيرك، بي إي، آر دي أولسون، وبي جيه كوساك، تجربة عشوائية مضبوطة للفيتويستروجين في العلاج الوقائي للصداع النصفي المرتبط بالحيض. العلاج الدوائي الحيوي، 2002. 56 (6): ص 283-8.
- إيكرمان-هارتر، ك.، وآخرون، كبح الأندروجين للاكتئاب المنتشر في فئران طافرة مصابة بالصداع النصفي الشقي العائلي من النوع 1. حوليات علم الأعصاب، 2009. 66 (4): ص. 564-8.
- نابي، ر. إي، ك. واورا، وس. شميت، اضطراب انخفاض الرغبة الجنسية لدى النساء بعد انقطاع الطمث. أمراض النساء والغدد الصماء، 2006. 22 (6): ص. 318-23.
- ماكجريجور، إي إيه، الصداع النصفي المرتبط بالحيض وما قبل انقطاع الطمث: مراجعة سردية. ماتوريتاس، 2020. 142 : ص 24-30.
- شورتسانيتيس، جي، وآخرون، التفاعلات الدوائية بين الأدوية النفسية وموانع الحمل الفموية. مجلة آراء الخبراء في استقلاب الأدوية وعلم السموم، 2022. 18 (6): ص 395-411.
- لازورويتز، أ.، وآخرون، تأثير توبيراميت على تركيزات إيتونوجيستريل في مصل الدم لدى مستخدمات غرسات منع الحمل. طب التوليد وأمراض النساء، 2022. 139 (4): ص. 579-587.
- أورنيلو، ر.، وآخرون، الصداع المرتبط بالحيض لدى النساء المصابات بالصداع النصفي المزمن المعالجات بالإيرينوماب: سلسلة حالات رصدية. علوم الدماغ، 2021. 11 (3).
- بافلوفيتش، جيه إم، وآخرون، فعالية وسلامة إيرينوماب لدى النساء اللواتي لديهن تاريخ من الصداع النصفي المرتبط بالحيض. مجلة الصداع والألم، 2020. 21 (1): ص 95.
- أدويي، إي أو، وآخرون، الآليات الجينية الجزيئية المشتركة الكامنة وراء مرض بطانة الرحم المهاجرة والصداع النصفي المصاحب. الجينات (بازل)، 2020. 11 (3).
- صادق، إس إي، وآخرون، خطر الإصابة بالسكتة الدماغية لدى النساء المصابات بالصداع النصفي، ارتباط خفي: مراجعة منهجية. كيوريوس، 2022. 14 (7): ص. e27103.
- سياو، دبليو زد، وآخرون، خطر الإصابة بمرض الشرايين المحيطية والسكتة الدماغية لدى مرضى الشقيقة المصحوبة أو غير المصحوبة بهالة: دراسة جماعية وطنية قائمة على السكان. المجلة الدولية للعلوم الطبية، 2022. 19 (7): ص. 1163-1172.
- شامبالو، إس دبليو، وآخرون، استخدام موانع الحمل الهرمونية المركبة لدى النساء المصابات بالصداع النصفي وخطر الإصابة بالسكتة الدماغية الإقفارية. المجلة الأمريكية لأمراض النساء والتوليد، 2017. 216 (5): ص. 489.e1-489.e7.
- إرشادات منع الحمل الهرموني الصادرة عن الجمعية الألمانية لأمراض النساء والتوليد (DGGG)، والجمعية الألمانية لأمراض النساء والتوليد (SGGG)، والجمعية الألمانية لأمراض النساء والتوليد (OEGGG) (المستوى S3، رقم التسجيل في AWMF: 015/015، نوفمبر 2019). https://register.awmf.org/de/leitlinien/detail/015-015.
- دينر، هـ.-ك.، وآخرون، علاج نوبات الصداع النصفي والوقاية منه، الدليل الإرشادي S1، 2022، DGN وDMKG ، في إرشادات التشخيص والعلاج في طب الأعصاب ، DGfN (محرر)، محرر. 2022: متاح على الإنترنت: www.dgn.org/leitlinien .
تنزيل ملف PDF: منشور طب الألم 02 2023










اترك تعليقًا