العديد من مناطق الدماغ ذات الصلة بالفيزيولوجيا المرضية للصداع النصفي ، وجهاز الأوعية الدموية القحفية ، ودورا الأم والقرن الخلفي لحبل الشوكة يعبر عن مستقبلات هرمون الاستروجين. هذا يعني أنه يمكن تعديل المحفزات المؤلمة. يمكن أن تحدث هجمات الصداع النصفي في علاقة زمنية بنافذة الحيض. الصداع النصفي هو عامل خطر للسكتة الدماغية وغيرها من الأحداث الوعائية. هناك أدلة مكثفة على أن زيادة خطر الإصابة بالسكتات الدماغية ترتبط مع كل من الصداع النصفي بدون هالة ومع الصداع النصفي مع الهالة. نظرًا لأن خطر الإصابة بالسكتة الدماغية يمكن أيضًا زيادة عند استخدام وسائل منع الحمل الهرمونية ، فإن السؤال مهم هو خيارات العمل في الممارسة العملية.
تصنيف الصداع النصفي فيما يتعلق بالحيض
الطبعة الثالثة الحالية من التصنيف الدولي للصداع ICHD3 [1]، مثل الإصدارات السابقة، لم تخصص أي مساحة في الجزء الرئيسي لنوبات الصداع النصفي التي تحدث فيما يتعلق بنافذة الدورة الشهرية. الطبعة الأولى في عام 1988 [2] لم تتضمن أي معايير رسمية للصداع النصفي المرتبط بالحيض. ولكن بالفعل في هذه الطبعة الأولى، تمت الإشارة في قسم التعليقات إلى أنه بالنسبة لبعض النساء، يمكن أن تحدث نوبات الصداع النصفي بدون هالة حصريًا أثناء الحيض. وكان هذا يسمى "ما يسمى بالصداع النصفي الحيضي". يجب استخدام المصطلح فقط إذا حدثت 90٪ على الأقل من النوبات في الفترة التي تسبق الدورة الشهرية بيومين وحتى اليوم الأخير من الدورة الشهرية. في الطبعة الثانية من التصنيف الدولي للصداع في عام 2004 [3]، تم تعريف نوعين فرعيين من الصداع النصفي المرتبط بالحيض لأول مرة في الملحق. يشير ما يسمى بـ "الصداع النصفي الحيضي النقي" إلى النوبات التي تحدث حصريًا فيما يتعلق بالدورة الشهرية. وعلى النقيض من ذلك، مع ما يسمى "الصداع النصفي المرتبط بالحيض"، تحدث الهجمات أيضًا في أوقات أخرى من الدورة. كان كلا الشكلين عبارة عن مجموعات فرعية حصرية من الصداع النصفي بدون هالة. يصف ملحق التصنيف الدولي للصداع معايير البحث الخاصة بأعراض الصداع التي لم يتم التحقق من صحتها بشكل كافٍ من خلال الدراسات العلمية. تشير كل من تجربة أعضاء لجنة تصنيف الصداع والمنشورات ذات الجودة المتفاوتة إلى وجود هذه الكيانات المدرجة في الملحق، والتي يمكن اعتبارها اضطرابات متميزة ولكن يجب تقديم المزيد من الأدلة العلمية قبل أن يتم قبولها رسميًا . إذا نجح ذلك، فيمكن دمج هذه التشخيصات من الملحق في الجزء الرئيسي في المرة التالية التي يتم فيها مراجعة التصنيف.
في الإصدار الثالث من التصنيف الدولي للصداع لعام 2018، لا يزال "الصداع النصفي الحيضي النقي" و"الصداع النصفي المرتبط بالحيض" موجودين فقط في الملحق. يتطلب كلا التشخيصين أن تحدث نوبات الصداع النصفي في اليوم 1 ± 2 من الدورة الشهرية (أي اليوم من −2 إلى +3) من الدورة الشهرية في دورتين من أصل 3 دورات شهرية على الأقل (الجدول 1، الشكل 1). ومع ذلك، فقد تم الآن توسيع المعايير لتشمل نوعًا فرعيًا به هالة، على الرغم من أن نوبات الصداع النصفي أثناء الحيض تحدث عادةً بدون هالات. هذا يحدد الصداع النصفي الحيضي النقي مع أو بدون هالة وكذلك الصداع النصفي المرتبط بالحيض مع أو بدون هالة. إذا تم الجمع بين أشكال الصداع النصفي الحيضي النقي والصداع النصفي المرتبط بالحيض، فإننا نتحدث بشكل جماعي عما يسمى "الصداع النصفي الحيضي" [4].
الجدول 1. معايير تشخيص ICHD-3 للصداع النصفي داخل وخارج نافذة الدورة الشهرية
———————————————————————————
A1.1.1 الصداع النصفي الحيضي بدون هالة
- الهجمات التي تصيب المرأة الحائض 1 التي تستوفي الصداع النصفي بدون هالة
- تحدث الهجمات حصريًا في اليوم 1 ± 2 (أي اليوم −2 إلى +3) من الحيض 1 في دورتين من أصل 3 دورات شهرية على الأقل وليس في أي وقت آخر من الدورة.
A1.1.2 الصداع النصفي المرتبط بالدورة الشهرية بدون هالة
- الهجمات التي تصيب المرأة الحائض التي تستوفي معايير 1.1 الصداع النصفي بدون هالة والمعيار ب أدناه
- تحدث الهجمات في اليوم 1 ± 2 من الحيض ( أي اليوم −2 إلى +3) من الحيض في دورتين من أصل 3 دورات شهرية على الأقل، ولكن أيضًا في أوقات أخرى من الدورة.
A1.1.3 الصداع النصفي غير الحيضي بدون هالة
- الهجمات التي تصيب المرأة الحائض التي تستوفي معايير 1.1 الصداع النصفي بدون هالة والمعيار B أدناه
- تستوفي المعيار B لـ A1.1.1 الصداع النصفي الحيضي المحض بدون هالة أو A1.1.2 الصداع النصفي المرتبط بالحيض بدون هالة
———————————————————————————
A1.2.0.1 الصداع النصفي الحيضي المصحوب بهالة
- الهجمات التي تصيب المرأة الحائض 1 التي تستوفي الصداع النصفي مع الهالة
- تحدث الهجمات في الأيام 1 ± 2 من الحيض (أي الأيام من −2 إلى +3) من الحيض في دورتين من أصل 3 دورات شهرية على الأقل، ولكن أيضًا في أوقات أخرى من الدورة.
A1.2.0.2 الصداع النصفي المصاحب للدورة الشهرية مع الهالة
- هجمات تصيب المرأة الحائض التي تستوفي الصداع النصفي مع الهالة
- تحدث الهجمات في اليوم 1 ± 2 من الحيض ( أي اليوم −2 إلى +3) من الحيض في دورتين من أصل 3 دورات شهرية على الأقل، ولكن أيضًا في أوقات أخرى من الدورة.
A1.2.0.3 الصداع النصفي غير الحيض مع هالة
- هجمات تصيب المرأة الحائض التي تستوفي الصداع النصفي مع الهالة
- تستوفي المعيار B لـ A1.2.0.1 الصداع النصفي الحيضي المصحوب بهالة أو A1.2.0.2 الصداع النصفي المرتبط بالحيض مع هالة
———————————————————————————
لأغراض ICHD-3، يعتبر الحيض نزيف بطانة الرحم الناتج عن الدورة الشهرية الطبيعية أو انسحاب المركبات بروجستيرونية المفعول الخارجية، وينطبق الأخير على موانع الحمل الفموية المشتركة والعلاج بالهرمونات البديلة الدورية (الشكل 1). وفقًا لـ ICHD-3، فإن التمييز بين الصداع النصفي الحيضي بدون هالة والصداع النصفي المرتبط بالحيض بدون هالة مهم لأن العلاج الوقائي بالهرمونات من المرجح أن يكون فعالاً في الأخير [1].
تشير أكثر من 50% من النساء المصابات بالصداع النصفي إلى وجود علاقة بين الدورة الشهرية والصداع النصفي [5]. يختلف معدل الانتشار في الدراسات المختلفة بسبب معايير التشخيص المختلفة. تتراوح نسبة انتشار الصداع النصفي الحيضي بدون هالة بين 7% و14% لدى مرضى الصداع النصفي، بينما تتراوح نسبة انتشار الصداع النصفي الحيضي بدون هالة بين 10% و71% لدى مرضى الصداع النصفي. يصاب حوالي واحد من كل ثلاثة إلى خمسة مرضى بالصداع النصفي بنوبة صداع نصفي بدون هالة مرتبطة بالحيض [5]. تميل العديد من النساء إلى المبالغة في العلاقة بين الدورة الشهرية ونوبات الصداع النصفي. ولأغراض البحث، يتطلب التشخيص أدلة موثقة مستقبليًا لما لا يقل عن ثلاث دورات كما يتضح من تطبيق الصداع النصفي أو سجلات اليوميات [1].
قد تختلف آليات الصداع النصفي اعتمادًا على ما إذا كان نزيف بطانة الرحم يحدث نتيجة للدورة الشهرية الطبيعية أو انسحاب البروجستينات الخارجية (كما هو الحال مع موانع الحمل الفموية المشتركة والعلاج بالهرمونات البديلة الدورية). تنتج الدورة الشهرية الداخلية من تغيرات هرمونية معقدة في محور منطقة ما تحت المهاد والغدة النخامية والمبيضين، مما يؤدي إلى تحفيز الإباضة، والتي بدورها يتم قمعها عن طريق تناول موانع الحمل الفموية المشتركة. ولذلك ينبغي النظر إلى هذه المجموعات السكانية الفرعية بشكل منفصل من الناحية الفيزيولوجية المرضية، على الرغم من أنه لا يمكن تمييز معايير التشخيص عن بعضها البعض.
هناك أدلة على أنه في بعض النساء على الأقل، قد تحدث نوبات الصداع النصفي أثناء الدورة الشهرية بسبب انسحاب هرمون الاستروجين، على الرغم من أن التغيرات الهرمونية أو البيوكيميائية الأخرى قد تكون ذات صلة أيضًا في هذه المرحلة من الدورة [4]. إذا كان الصداع النصفي الحيضي النقي أو الصداع النصفي المرتبط بالحيض مرتبطًا بانسحاب هرمون الاستروجين الخارجي، فيجب إجراء كلا التشخيصين، الصداع النصفي الحيضي النقي بدون هالة أو الصداع النصفي المرتبط بالدورة الشهرية بدون هالة وصداع انسحاب هرمون الاستروجين. يمكن أن يتغير الارتباط بالحيض على مدار العمر الإنجابي للمرأة.
تأثير الهرمونات على الصداع
تم تضمين تأثير الهرمونات على الصداع في القسم الرئيسي "الصداع الثانوي" في الطبعة الثانية لعام 2004 (ICHD-2) من التصنيف الدولي للصداع [3]. تتعلق المعايير بالصداع الذي حدث مؤخرًا بسبب تناول الهرمونات أو الصداع الموجود مسبقًا والذي تفاقم نتيجة لذلك. وتتطلب المعايير أن يتحسن الصداع بعد توقف الهرمونات أو أن يتكرر النمط السابق في حالة الصداع الموجود مسبقًا.
في الطبعة الثالثة 2018 (ICHD-3) [1]، كان وجود الصداع لمدة 15 يومًا على الأقل شهريًا مطلوبًا لتشخيص الصداع المنسوب إلى تناول الهرمونات الخارجية. يتطلب تشخيص صداع انسحاب هرمون الاستروجين وفقًا لـ ICHD-3 أن يبدأ الصداع خلال 5 أيام من توقف هرمون الاستروجين إذا تناولت النساء هرمون الاستروجين لمدة ثلاثة أسابيع على الأقل أو أكثر.
الاستروجين والصداع النصفي
في عام 1972، وصف سومرفيل أن الحقن العضلي قبل الدورة الشهرية مباشرة لاستراديول فاليرات، وهو استر مساعد للدواء من 17 بيتا استراديول، يمكن أن يؤخر ظهور نوبة الصداع النصفي المرتبطة بالدورة الشهرية [6]. تم تحديد الحد الأدنى لتركيز 17-β-استراديول في الدورة الدموية بنسبة 45-50 بيكوغرام/مل، والذي يمكن أن يؤدي دونه إلى حدوث نوبة الصداع النصفي. وكانت هذه العتبة واضحة أيضًا عند النساء في سن اليأس اللاتي خضعن للعلاج بالهرمونات البديلة باستخدام استراديول 17 بيتا العضلي. بناءً على هذه البيانات، تم الافتراض بأن نوبات الصداع النصفي في فترة الحيض تنجم عن انخفاض هرمون الاستروجين. وبناءً على ذلك، تم الافتراض بأن تقلبات هرمون الاستروجين الفسيولوجية تلعب دورًا في تطور الصداع النصفي. تم دعم هذا الافتراض من خلال اكتشاف أن قابلية معينة لنوبات الصداع النصفي تحدث أثناء انخفاض هرمون الاستروجين في المرحلة الصفراء المتأخرة. ومع ذلك، لا يمكن إثبات الاختلافات في القيم القصوى أو متوسط قيمة التركيز اليومي للإستروجين أثناء دورات الإباضة لدى مرضى الصداع النصفي مقارنة بالضوابط الصحية [4، 7].
الاستروجين والجهاز العصبي
الاستروجين الداخلي الأكثر صلة هو 17β-استراديول [8]. لديه إمكانية الوصول إلى الجهاز العصبي المركزي من خلال الانتشار السلبي عبر حاجز الدم في الدماغ. ومع ذلك، يمكن أيضًا تصنيعه محليًا في الدماغ من الكوليسترول أو من السلائف العطرية بواسطة إنزيم أروماتيز ويعمل هناك كستيرويد عصبي. قد تكون التأثيرات الفسيولوجية ناجمة عن تنشيط مستقبلات هرمون الاستروجين المختلفة، وخاصة مستقبلات هرمون الاستروجين α (ERα)، ومستقبل هرمون الاستروجين β (ERβ)، ومستقبل هرمون الاستروجين المقترن بالبروتين G-1 (GPER / GPR30) [9].
يطور هرمون الاستروجين تأثيراته البيولوجية في الجهاز العصبي المركزي من خلال الآليات الخلوية الجينومية أو غير الجينية. هذا يمكن أن يغير النقل العصبي ووظيفة الخلية. يمكن لشلالات الإشارات داخل الخلايا تعديل التفاعلات الأنزيمية، وتوصيل القنوات الأيونية، واستثارة الخلايا العصبية [4].
العديد من مناطق الدماغ المشاركة في الفيزيولوجيا المرضية للصداع النصفي تعبر عن مستقبلات هرمون الاستروجين. وينطبق هذا بشكل خاص على منطقة ما تحت المهاد، والمخيخ، والجهاز الحوفي، والنواة الجسرية والرمادية المحيطة بالمسالي (المادة الرمادية المحيطة بالمجاري). يتم التعبير عن مستقبلات هرمون الاستروجين أيضًا في القشرة الدماغية، والتي يمكنها تعديل حساسية الألم بشكل واضح وفعال. كما يعبر نظام الأوعية الدموية القحفية والأم الجافية والقرن الظهري للحبل الشوكي عن مستقبلات هرمون الاستروجين، والتي يمكن أن تعدل المنبهات المؤلمة [4، 8، 9].
أظهرت دراسات الارتباط على مستوى الجينوم عدم وجود علاقة بين تعدد أشكال مستقبلات هرمون الاستروجين وزيادة خطر الإصابة بالصداع النصفي. ومع ذلك، فقد وجد أن تعدد الأشكال النووي في جين SYNE1 يرتبط بالصداع النصفي الحيضي [10].
يمكن تنشيط نظام السيروتونين عن طريق هرمون الاستروجين، والذي يمكن أن يكون له تأثير وقائي ضد نوبات الصداع النصفي [11]. يمكن أن يزيد الإستروجين أيضًا من التأثيرات المثيرة للغلوتامات. وهذا قد يفسر زيادة احتمال ظهور هالة الصداع النصفي خلال فترات تركيزات هرمون الاستروجين العالية، مثل أثناء الحمل أو عند تلقي الهرمونات الخارجية.
يمكن للإستروجين تعديل نظام حمض جاما أمينوبوتيريك (GABA)، والذي له تأثير مثبط في الجهاز العصبي [12]. يمكن للبروجستيرون، الذي يتم إنتاجه بشكل رئيسي عن طريق الجسم الأصفر للمبيضين، ومستقلبه الألوبريجنانولون أن يعزز نشاط GABAergic وبالتالي يسبب تأثيرًا مضادًا للألم.
يمكن للإستروجين أيضًا تعديل نظام المواد الأفيونية الذاتية من خلال زيادة تخليق الإنكيفالين [13]. وبناءً على ذلك، قد يكون انخفاض مستويات هرمون الاستروجين والبروجستيرون خلال المرحلة الصفراء المتأخرة مرتبطًا بانخفاض تنشيط النظام الأفيوني. وهذا يسبب زيادة الحساسية للألم. أظهرت الدراسات التي أجريت على حساسية الألم خلال المراحل المختلفة من الدورة الشهرية زيادة الحساسية خلال المرحلة الأصفرية، خاصة عند النساء اللاتي يشتكين من أعراض ما قبل الحيض [14]. تعمل التركيزات العالية من هرمون الاستروجين أيضًا على تعزيز تكوين الناقلات العصبية والببتيدات العصبية الأخرى المثبطة للألم، مثل الببتيد العصبي Y والبرولاكتين والفاسوبريسين، والتي يمكن أن تلعب دورًا في تطور الصداع النصفي [4].
الأوكسيتوسين والصداع النصفي
يتكون الأوكسيتوسين العصبي في ما تحت المهاد. لها آثار واسعة في الجهاز العصبي المركزي. على وجه الخصوص ، فإنه يعدل المزاج والسلوك. إنه يؤثر على التحكم في الألم في الجسم ويمكن أن يكون له تأثير محدد للصداع النصفي [4]. كما يتم زيادة مرايا الأوكسيتوسين في مراحل زيادة تركيزات الاستروجين. يؤدي هرمون الاستروجين إلى زيادة إنتاج الأوكسيتوسين في ما تحت المهاد ومناطق الدماغ الأخرى ، وخاصة في نواة مثلث التوائم [15]. تُظهر النساء اللائي يعانين من الصداع النصفي الحيض عتبات الألم المهينة خلال المرحلة الخالية من الهرمونات عند إعطاء وسائل منع الحمل الهرمونية المشتركة ، أي في الوقت الذي قلل من تركيزات هرمون الاستروجين [16].
ترتبط الفيزيولوجيا المرضية للصداع النصفي بزيادة نشاط مسبب للألم القشري في نظام مسبب للألم ثلاثي التوائم. وهذا يسبب توسع الأوعية الدموية داخل الجمجمة والتهاب السحايا [15]. قد يؤدي التنشيط المحلي لمستقبلات هرمون الاستروجين في العقدة الثلاثية التوائم إلى إثارة نوبات الصداع النصفي. لدى النساء مستقبلات هرمون الاستروجين في العقدة الثلاثية التوائم أكثر من الرجال [17]. يمكن أن يؤثر هرمون الاستروجين بشكل حاد على قوة الأوعية الدموية عن طريق تثبيط قنوات الكالسيوم في العضلات الملساء [18]. يمكن أيضًا تنشيط الاكتئاب القشري المنتشر (CSD) بواسطة هرمون الاستروجين. يؤدي هذا إلى إزالة الاستقطاب العصبي القشري، والذي يعتبر سمة مميزة للصداع النصفي مع الهالة [19]. المستويات العالية من هرمون الاستروجين تزيد من القابلية للإصابة بـ CSD، كما أن انسحاب الإستروجين يقلل من القابلية للإصابة بـ CSD. قد يفسر هذا سبب ارتباط نوبات الصداع النصفي في فترة الدورة الشهرية بالهالة [1].
هرمون الاستروجين والببتيدات المرتبطة بالجينات الكالسيتونين (CGRP)
يعتبر الآن إطلاق الببتيد المرتبط بجين الكالسيتونين (CGRP) خطوة حاسمة في الفيزيولوجيا المرضية للصداع النصفي. يمكن أن يؤدي تحفيز العقدة الثلاثية التوائم إلى إطلاق CGRP والمادة P في الدورة الدموية في الجمجمة [20]. ينشط CGRP آليات مسببة للألم في الجافية، والعقدة الثلاثية التوائم، ومجمع نواة عنق الرحم الثلاثي التوائم، والمهاد والرمادي حول القناة، من بين أمور أخرى [20]. يمكن حظر كل من الأعراض السريرية للصداع النصفي وإطلاق CGRP بواسطة أدوية التريبتان [21]. يمكن أن يؤدي حقن CGRP إلى إثارة نوبة لدى مرضى الصداع النصفي [22]. هذا ليس هو الحال في الضوابط الصحية. الأجسام المضادة وحيدة النسيلة التي تستهدف على وجه التحديد CGRP باعتبارها يجند (eptinezumab و fremanezumab و galcanezumab) أو مستقبل CGRP (erenumab) متاحة الآن في الرعاية الصحية للعلاج الوقائي للصداع النصفي العرضي والمزمن [23، 24]. لقد ثبت أنها فعالة ومقبولة في الدراسات الخاضعة للرقابة.
مستويات CGRP أعلى في النساء مقارنة بالرجال [25]. كما أنها تربى أثناء الحمل وهدية من وسائل منع الحمل الهرمونية المشتركة. في انقطاع الطمث ، المرايا متغيرة [26]. يتم التعبير عن مستقبلات CGRP ومستقبلات هرمون الاستروجين في نفس مناطق الدماغ. يمكن أن يعدل هرمون الاستروجين إنتاج CGRP في الخلايا العصبية التوائم. من الناحية التجريبية ، يؤدي إدارة الاستروجين الخارجي إلى انخفاض مرايا CGRP [27]. خلال فترة ما بعد انقطاع الطمث ، يمكن زيادة مستويات CGRP ، في حين يتم تقليل تركيزات هرمون الاستروجين [28].
باعتبارها ببتيدًا عصبيًا نشطًا في الأوعية، يمكن أن تسبب المادة P أيضًا التهابًا عصبيًا في السحايا فيما يتعلق بالصداع النصفي [28]. قد يؤدي تناول هرمون الاستروجين إلى تقليل مستويات البلازما للمادة P. باختصار، يمكن للإستروجين تعديل كل من CGRP والمادة P من خلال التأثيرات المثبطة. ولذلك يوفر الإستروجين آلية وقائية ضد الالتهاب العصبي [28]. بالإضافة إلى ذلك، يمكن أن يثبط هرمون الاستروجين التأثير المنشط للبروجستيرون على CGRP والمادة P. يشير هذا إلى أن مزيج الاستروجين والبروجستيرون له تأثير مثبت على CGRP وإطلاق المادة P [4].
زاد مرضى الصداع النصفي من المرايا من السيتوكينات الالتهابية المحترفين أثناء هجوم الصداع النصفي وفي الفاصل الزمني [29]. تشير الدراسات التجريبية إلى أن الجزيئات الالتهابية للاستروجين يمكن أن تمنع. بالإضافة إلى ذلك ، لديهم وقائي ضد الالتهاب الناجم عن البروستاجلاندين. في المقابل ، يمكن أن يؤدي انسحاب هرمون الاستروجين إلى زيادة حساسية البروستاجلاندين وتنشيط الالتهاب العصبي عن طريق زيادة إطلاق الببتيدات العصبية مثل CGRP والمادة P و Neurokinine [30].
باختصار، تشير البيانات المتاحة إلى أن هرمون الاستروجين في حد ذاته ليس له تأثير وقائي مباشر على نوبات الصداع النصفي. ومع ذلك، يمكن أن يؤثر الإستروجين بشكل غير مباشر على تنشيط وتثبيط عوامل الصداع النصفي. ونتيجة لذلك، يمكن منع بدء نوبات الصداع النصفي في منطقة الأوعية الدموية العصبية. في الدورة الدموية الثلاثية التوائم، يمكن تقليل الحساسية للصداع النصفي. إذا انخفضت تركيزات هرمون الاستروجين، يمكن خفض عتبة نوبات الصداع النصفي [4، 15].
هرمون الاستروجين في الوقاية من الصداع النصفي الحيض
في بعض المرضى، قد تحدث نوبات الصداع النصفي فقط خلال فترة الحيض [1]. يمكن أن يكون للنوبات خصائص ألم أكثر شدة (المدة والشدة والتفاقم بسبب النشاط البدني) والأعراض المصاحبة (الغثيان والقيء ورهاب الضوء ورهاب الصوت) مقارنة بنوبات الصداع النصفي خارج فترة الدورة الشهرية.
يمكن أن يكون تأثير تركيزات هرمون الاستروجين الطبيعية وسيلة لمنع هجمات الصداع النصفي المرتبطة من قبل الرجال. الهدف من ذلك هو الحد من تقلبات التركيز الهرموني وإهدار هرمون الاستروجين خلال مرحلة نزيف الحيض. ويستند ذلك إلى الملاحظة التي تشير إلى أن حساسية هجمات الصداع النصفي خلال النافذة المحيطية بين اليوم -2 و +3 من الحيض ترتبط مع انخفاض الهرمونات [31].
في الأساس ، يتوفر إجراءان لاستخدام الهرمونات في المعالجة الوقائية للصداع الصداع الوطني:
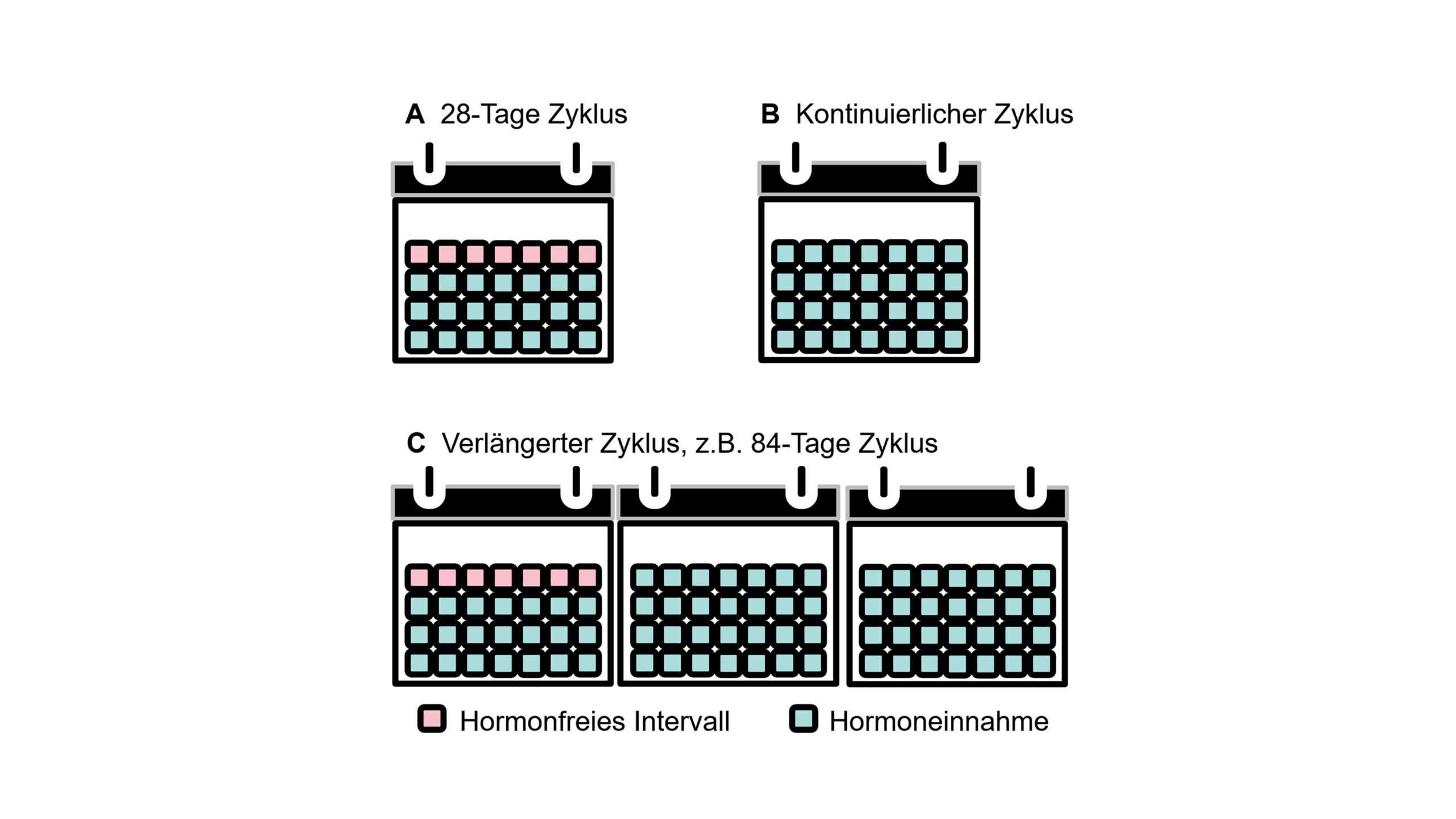
- يمكن استخدام وسائل منع الحمل الهرمونية مع مخططات إدارة مختلفة من الإيثينيلستراديول اعتمادًا على مدة الفاصل الخالي من الهرمون. يتضمن الإجراء المخطط القياسي 21/7 ، والمخططات الموسعة المتغيرة والمخططات المستمرة دون فترات خالية من الهرمونات (الشكل 2). تشمل خيارات التطبيق موانع الحمل الهرمونية الفموية والحلقات المهبلية.
- يمكن أيضًا استخدام مكملات الاستروجين غير المصممة لمنع الحمل. تشمل الأمثلة اللصقات عبر الجلد وتطبيقات الجل والغرسات تحت الجلد. وتهدف هذه إلى التعويض عن انخفاض هرمون الاستروجين خلال فترة ما حول الدورة الشهرية في الصداع النصفي المرتبط بالدورة الشهرية والصداع النصفي الحيضي النقي.
البيانات المتعلقة باستخدام الهرمونات في الوقاية من الصداع النصفي الحيضي محدودة للغاية ومتناقضة في بعض الأحيان. الأساس المنطقي هو التعويض عن انخفاض هرمون الاستروجين الداخلي لدى المرضى الذين يعانون من الصداع النصفي الحيضي النقي مع الحيض المتوقع [4، 32، 33]. من ناحية أخرى، يهدف الإدارة المستمرة لجرعات منخفضة إلى مواجهة التقلبات الهرمونية الفسيولوجية. يهدف الاستخدام المشترك للإستروجين والجيستاجين إلى تثبيت مستويات الهرمون وتمكين منع الحمل [4، 32، 33]. فيما يلي وصف للخيارات المختلفة للتأثير على الدورة الهرمونية الأنثوية لعلاج الصداع النصفي.
ديسوجيستريل (دواء يحتوي على البروجستين فقط)
تم فحص تأثير ديسوجيستريل 75 ميكروغرام يوميًا لدى النساء المصابات بالصداع النصفي مع أو بدون هالة في أربع دراسات مراقبة مفتوحة [34-37]. وقد فحصت الدراسة النساء اللاتي تناولن الدواء إما لمنع الحمل أو لأسباب طبية، ولكن ليس للوقاية من الصداع النصفي. تشمل الآثار الجانبية لاستخدام ديسوجيستريل زيادة الصداع وطول مدة النزيف والتبقيع وحب الشباب. في المقابل، هناك أدلة محدودة فقط على فعالية ديسوجيستريل على مسار الصداع النصفي لدى النساء المصابات بالصداع النصفي بدون هالة أو الصداع النصفي مع هالة. يمكن أخذ ديسوجيستريل في الاعتبار في ضوء المخاطر القلبية الوعائية المواتية لدى النساء اللاتي يعانين من الصداع النصفي مع أو بدون هالة وعوامل الخطر الإضافية للأوعية الدموية.
وسائل منع الحمل عن طريق الفم مجتمعة
وضع الدراسة الحالي للاستخدام المطول لوسائل منع الحمل المركبة عن طريق الفم لدى النساء المصابات بالصداع النصفي محدود [4، 32]. هنا أيضًا، لا توجد سوى دراسات مراقبة مفتوحة تم إجراؤها على النساء اللاتي تناولن المادة الفعالة لمنع الحمل أو لأسباب طبية - وليس للوقاية من الصداع النصفي. استخدمت دراسة واحدة فقط موانع الحمل الفموية المركبة خصيصًا للوقاية من الصداع [38]. تشير البيانات المتاحة إلى فائدة محتملة للاستخدام طويل الأمد لوسائل منع الحمل الهرمونية المركبة لدى النساء المصابات بالصداع النصفي بدون هالة.
ديسوجيستريل مقابل الإدارة الموسعة لموانع الحمل الفموية المشتركة
في الدراسات الرصدية المفتوحة التسمية، تمت مقارنة تأثير الحبة الصغيرة من ديسوجيستريل مع تناول موانع الحمل الفموية المركبة لفترة طويلة في الصداع النصفي بدون هالة. في دراسة أجراها موروتي وآخرون [36] لم يكن هناك اختلاف في أيام الصداع النصفي وأيام الصداع وشدة الصداع وأيام استخدام التريبتان. الدراسات الحالية التي تقارن حبوب منع الحمل الصغيرة ديسوجيستريل مع وسائل منع الحمل عن طريق الفم مجتمعة محدودة. لا تسمح نتائج الدراسات الرصدية بالإدلاء بأي بيانات قاطعة حول الفعالية.
وسائل منع الحمل عن طريق الفم مجتمعة مع فاصل زمني خالٍ من حبوب منع الحمل
لا توجد أيضًا سوى دراسات ذات جودة منخفضة فيما يتعلق باستخدام موانع الحمل الفموية المدمجة مع فاصل زمني خالٍ من الحبوب [4، 32]. هذه لديها مخططات غير متجانسة للغاية. لا يوجد دليل على تفوق أي نظام محدد مقارنة بالخيارات الأخرى. لا توجد أدلة كافية لاستخدام العلاج فقط للوقاية من الصداع النصفي. في بعض النساء، كان لا بد من وقف الجرعة في وقت مبكر بسبب تفاقم الصداع النصفي.
وسائل منع الحمل عن طريق الفم مجتمعة مع إعطاء هرمون الاستروجين عن طريق الفم خلال "فترة خالية من حبوب منع الحمل"
الأدلة على استخدام وسائل منع الحمل الهرمونية المركبة عن طريق الفم مع استبدال هرمون الاستروجين عن طريق الفم خلال فترة خالية من حبوب منع الحمل متاحة فقط من دراسة واحدة [39]. لا تسمح البيانات الحالية بالإدلاء بأي بيانات حول فعالية نظام العلاج هذا في سياق الصداع النصفي.
وسائل منع الحمل عن طريق الفم مجتمعة مع مكملات استراديول من خلال التصحيح خلال فترة خالية من حبوب منع الحمل
في دراسة مركزية واحدة، لم يكن هناك انخفاض كبير في عدد أيام الصداع النصفي، وشدة الصداع النصفي، والأعراض المرتبطة بالصداع النصفي [40]. وشملت الأحداث السلبية المرتبطة بمكملات استراديول عبر الجلد نزيف الانسحاب المتغير. لا توفر البيانات الحالية مبررًا كافيًا لاستخدام مكملات الاستراديول مع الرقع لمنع الصداع النصفي خلال الفترة الخالية من الحبوب.
لصقات منع الحمل الهرمونية المركبة
وضع البيانات لاستخدام اللصقات المختلطة الهرمونية المدمجة محدودة للغاية. البيانات متاحة فقط من دراسة [41]. تشير نتائج هذه الدراسة إلى وجود صلة بين انسحاب الهرمونات والصداع. كانت أيام الصداع أعلى خلال الأسبوع بدون تصحيح. بعد تمديد الرصيف بعد العلاج الممتد ، لم يزداد تواتر الصداع. لا يبرر حالة الدراسة الحالية دليلًا على استخدام هذا الإجراء.
حلقة مهبلية هرمونية مجمعة لمنع الحمل
إن استخدام وسائل منع الحمل الهرمونية المدمجة مع حلقة مهبلية إلى مسار الصداع النصفي محدود للغاية [42]. البيانات المتاحة ليست كافية لتبرير الاستخدام لمنع الصداع النصفي [4 ، 32].
مكملات استراديول عبر الجلد مع هلام
تم فحص تأثير مكملات استراديول عبر الجلد مع هلام في المرضى قبل انقطاع الطمث في 3 دراسات [43-45]. تم استخدام استراديول جل 1.5 ملغ لمدة 6 أو 7 أيام. وتمت مقارنة التأثير مع إعطاء الدواء الوهمي. تم تصميم العلاج في الدراسة خصيصًا لمنع الصداع. لم يتم الإبلاغ عن الأحداث السلبية الخطيرة المرتبطة باستخدام هلام استراديول. تم توثيق الطفح الجلدي أو القلق أو انقطاع الطمث كأحداث سلبية. بناءً على الوضع الحالي للدراسة، لا يمكن تبرير استخدام استراديول عبر الجلد مع الجل للوقاية من الصداع النصفي بشكل كافٍ. من ناحية، فإن إعطاء استراديول عبر الجلد مع الجل أمر سهل وجيد التحمل بشكل عام. من ناحية أخرى، إذا كانت الدورة الشهرية لديك غير منتظمة، فقد يكون توقيت التطبيق مشكلة. يمكن أن تكون زيادة الصداع النصفي بسبب تأخر انسحاب هرمون الاستروجين غير مواتية أيضًا. قد يكون هذا بسبب زيادة تناول الاستراديول مع مكملات الاستراديول الإضافية وزيادة النفايات. يمكن أيضًا تثبيط الزيادة الجريبية في هرمون الاستروجين الداخلي عن طريق الإدارة الخارجية. نظرًا لنقص البيانات، لا يمكن حاليًا التوصية باستخدام هلام الإستروجين للوقاية من الصداع النصفي الناتج عن الدورة الشهرية. يمكن حاليًا النظر في هذا النهج إذا لم تكن جميع الاستراتيجيات الأخرى فعالة بما فيه الكفاية في الوقاية من الصداع النصفي الناتج عن الدورة الشهرية.
مكملات استراديول عبر الجلد من خلال التصحيح
الأدلة لاستخدام مكملات استراديول عبر الجلد مع التصحيح لعلاج الصداع النصفي الحيض محدودة. الأساس المنطقي للاستخدام هو الحفاظ على تركيزات استراديول مستقرة قبل بدء النزيف [41]. لا توجد حاليًا أي بيانات تثبت فعالية مكملات الاستراديول مع الرقع على مسار الصداع النصفي.
مكملات هرمون الاستروجين عبر الجلد مع اللصقات لدى النساء المصابات بانقطاع الطمث المستحث صيدلياً
لا يمكن تبرير استخدام استراديول عبر الجلد مع رقعة لدى النساء المصابات بانقطاع الطمث المستحث دوائيًا بشكل كافٍ بناءً على البيانات الحالية. أثناء انقطاع الطمث المستحث دوائيًا، يزداد خطر الإصابة بهشاشة العظام، والاكتئاب، والهبات الساخنة، والتهيج، وانخفاض الرغبة الجنسية، وجفاف المهبل. يمكن تقليل ذلك عن طريق العلاج بمكملات الإستروجين [46]. وضع الدراسة الحالي ليس كافيا لتبرير استخدامه للوقاية من الصداع النصفي.
زرع هرمون الاستروجين تحت الجلد مع البروجستيرون الحلقي
تم فحص استخدام غرسة الاستروجين تحت الجلد مع البروجستيرون الحلقي في دراسة رصدية مفتوحة [47]. لا يسمح وضع البيانات باستخلاص استنتاجات كافية للاستخدام المحتمل للوقاية من الصداع النصفي.
العلاج الإضافي
تم فحص مسار الصداع لدى النساء اللاتي تلقين نظير الهرمون المطلق لموجهة الغدد التناسلية (GnRH)، وهو محفز لانقطاع الطمث علاجي المنشأ المؤقت، بالإضافة إلى بقع هرمون الاستروجين عبر الجلد، بمفرده أو بالاشتراك مع البروجستيرون (العلاج الإضافي) [48]. كان هناك انخفاض في شدة الصداع، ولكن ليس تكرار الصداع. تقدم هذه الدراسة دليلاً على أن تقليل التقلبات الهرمونية قد يكون مفيدًا في الوقاية من الصداع النصفي خارج فترة الدورة الشهرية.
فيتويستروغنز
فيتويستروغنز هي مواد نباتية ثانوية مثل الايسوفلافون والقشور. وهي ليست هرمون الاستروجين بالمعنى الكيميائي، ولكن لها أوجه تشابه هيكلية معها. وهذا يؤدي إلى تأثير استروجين ضعيف أو مضاد للاستروجين. أشهر أنواع الاستروجين النباتي هي الايسوفلافون جينيستين والدايدزين والكوميسترول. يتم استخدام جينيستين ودايدزين على وجه الخصوص لتخفيف الهبات الساخنة وأعراض انقطاع الطمث الأخرى وكذلك للصداع النصفي الناتج عن الدورة الشهرية. أظهرت دراسة مفتوحة على مدى 10 أيام في فترة الحيض من -7 إلى +3 انخفاضًا متوسطًا في أيام الصداع بنسبة 62٪ [49]. أبلغ نصف المرضى عن عدم وجود غثيان وقيء مرتبط بالصداع النصفي. أكدت تجربة معشاة ذات شواهد التأثير على مدار 24 أسبوعًا من العلاج باستخدام 60 ملجم من أيسوفلافون الصويا، و100 ملجم من دونج كاي، و50 ملجم من الكوهوش الأسود. كان هناك انخفاض كبير للغاية في الصداع النصفي الحيضي، واستخدام الأدوية الحادة وشدة الصداع. لذلك يمكن أن يكون فيتويستروغنز خيارًا للنساء اللاتي لا يرغبن في تناول العلاجات الهرمونية أو لا يمكنهن استخدامها بسبب موانع الاستعمال، مثل أولئك اللاتي لديهن مخاطر كبيرة على القلب والأوعية الدموية.
مزيد من العلاجات الهرمونية
أظهرت الدراسات التي أجريت على استخدام خيارات منع الحمل لمنع الصداع أن تحفيز انقطاع الطمث يرتبط بتخفيف كبير للصداع [4، 32]. العلاجات التي تحتوي على مستحضرات البروجسترون فقط لديها خطر أقل لأحداث أو مضاعفات القلب والأوعية الدموية من هرمون الاستروجين [4، 30، 33]. يمكن أن تكون هذه أيضًا فعالة في الوقاية من الصداع النصفي المصحوب بالهالة. بسبب تناوله المستمر، لا تحدث تقلبات نموذجية في الهرمونات الجنسية الأنثوية والانسحاب الحاد من هرمون الاستروجين.
يظهر التستوستيرون قمع الاكتئاب المنتشر القشري في الدراسات قبل السريرية [51]. يمكن أن يؤدي إعطاء غرسات التستوستيرون تحت الجلد إلى تقليل شدة الصداع لدى المرضى الذين يعانون من قصور الأندروجين. بعد استئصال المبيض مع نقص الأندروجين، أبلغت النساء عن زيادة في تكرار الصداع النصفي مقارنة بالنساء اللائي يدخلن سن اليأس الطبيعي [52].
تعاني النساء اللاتي يخضعن للعلاج بالهرمونات البديلة أثناء انقطاع الطمث من تفاقم الصداع لديهم [53]. ربما يكون هذا بسبب الإطلاق غير المنتظم لهرمون الاستروجين. قد يكون العلاج بالهرمونات البديلة قادرًا على تثبيت انسحاب هرمون الاستروجين في هذه الحالة. يجب اختيار أقل جرعة ممكنة يمكنها التحكم في الأعراض أثناء انقطاع الطمث لتجنب الآثار الجانبية على القلب والأوعية الدموية، خاصة في الصداع النصفي المصحوب بهالة. قد يكون تطبيق هرمون الاستروجين عبر الجلد أو استخدام الأنظمة المركبة المستمرة مثل العلاج بالهرمونات البديلة الذي يتجنب النزيف هو أفضل طريقة لمنع الصداع النصفي في هذه الحالة.
توبيراميت والصداع النصفي الحيضي ومنع الحمل
تمت الموافقة على توبيراميت للعلاج الوقائي للصداع النصفي ويستخدم أيضًا للصداع النصفي الناتج عن الدورة الشهرية. في الجرعات اليومية من توبيراميت أعلى من 200 ملغ، ينبغي أن تؤخذ في الاعتبار إمكانية انخفاض فعالية وسائل منع الحمل وزيادة النزيف الاختراقي إذا استخدم المرضى وسائل منع الحمل عن طريق الفم مع وسائل منع الحمل الهرمونية مجتمعة [54]. يجب أن يُطلب من النساء اللاتي يتناولن وسائل منع الحمل المحتوية على هرمون الاستروجين الإبلاغ عن أي تغييرات في نزيف الدورة الشهرية إلى الطبيب. يمكن تقليل فعالية وسائل منع الحمل عن طريق العلاج بالتوبيراميت حتى في حالة عدم وجود نزيف اختراقي [55].
CGRP mAb والصداع النصفي الحيضي
لا يوجد حاليا أي علاج وقائي محدد لمؤشر الصداع النصفي الحيضي. في الآونة الأخيرة، تم دراسة استخدام الأجسام المضادة وحيدة النسيلة ضد CGRP أو مستقبل CGRP لعلاج الصداع النصفي الحيضي. نظرًا لنصف عمرها الطويل، تتمتع هذه بميزة أنها تحتاج فقط إلى تطبيقها شهريًا أو على فترات 3 أشهر، خاصة على المدى الطويل. Galcanezumab وerenumab وeptinezumab وfremanezumab متوفرون الآن في ألمانيا للعلاج الوقائي للصداع النصفي. في دراسة أجريت على إيرنيوماب [56]، تمت مقارنة مسار الصداع النصفي الحيضي في المجموعة التي استجابت للإرينوماب وفي المجموعة التي لم تستجب للإرينوماب. وقد وجد أن تكرار الصداع في كلا المجموعتين كان أكبر داخل نافذة الدورة الشهرية منه خارج نافذة الدورة الشهرية. وهذا يعني أنه حتى مع العلاج بدواء إرينوماب، فإن الصداع النصفي يحدث في كثير من الأحيان في نافذة الدورة الشهرية أكثر من خارج نافذة الدورة الشهرية. دراسة أخرى حللت فعالية erenumab في الوقاية من الصداع النصفي الحيض [57]. وشملت أيام الصداع النصفي الشهرية كلا من نوبات الصداع النصفي في الفترة المحيطة بالدورة الشهرية وبين فترات الحيض. أدى إرينوماب 70 ملغ و140 ملغ إلى خفض تواتر أيام الصداع النصفي شهريًا بشكل ملحوظ مقارنةً بالعلاج الوهمي. تدعم البيانات فعالية erenumab في الوقاية من الصداع النصفي الحيضي [57].
خطر القلب والأوعية الدموية
يعاني المصابون بالصداع النصفي من خطر الإصابة بالسكتة الدماغية بنسبة تقارب الضعف مقارنة بالأشخاص الأصحاء. هذا ينطبق بشكل خاص على الصداع النصفي مع الهالة. الصداع النصفي هو عامل خطر مهم للسكتة الدماغية مثل أهبة التخثر، الثقبة البيضوية الواضحة، تشريح الشرايين، التدخين والسمنة [4، 30، 32، 33، 58-60].
يعمل هرمون الاستروجين على تحسين تدفق الدم المعتمد على بطانة الأوعية الدموية وملامح الدهون. ومع ذلك، لديهم أيضًا تأثيرات تخثرية والتهابية. قد تكون هذه ذات أهمية خاصة في المرضى الذين هم في خطر متزايد للإصابة بالسكتة الدماغية وغيرها من الأحداث الوعائية مثل الأزمة القلبية أو تجلط الأوردة العميقة. قد يرتبط تناول موانع الحمل الفموية المركبة على وجه الخصوص ببداية مبكرة للسكتة الدماغية [4، 32، 61، 62].
من حيث المبدأ، يجب النظر بعناية في وجود عاملي خطر مستقلين للسكتة الدماغية. تشير الدراسات إلى أن النساء المصابات بالصداع النصفي ويتناولن أيضًا وسائل منع الحمل الهرمونية المركبة لديهن خطر متزايد للإصابة بالسكتة الدماغية بنسبة 2.1-13.9 [33، 61]. يرتبط خطر الإصابة بالسكتة الدماغية بجرعة الإستروجين. إرشادات الخبراء من الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH) [32، 33] والجمعية الألمانية لطب الأعصاب (DGN) بالتعاون مع الجمعية الألمانية للصداع النصفي والصداع [63] و لذلك لا توصي الجمعية الألمانية لأمراض النساء والتوليد [62] باستخدام وسائل منع الحمل الهرمونية المركبة للمرضى الذين يعانون من الصداع النصفي المصحوب بهالة. يجب على المرضى الذين يعانون من الصداع النصفي بدون هالة عدم استخدام وسائل منع الحمل الهرمونية المركبة في حالة وجود عوامل خطر وعائية أخرى. بدلا من ذلك، يمكن النظر في وسائل منع الحمل التي تحتوي على البروجستيرون فقط أو وسائل منع الحمل عن طريق الفم مجتمعة مع جرعات هرمون الاستروجين أقل من 35 ميكروغرام.
للوقاية من الصداع النصفي الناتج عن الدورة الشهرية، يمكن استخدام أنظمة الدورة الممتدة والتطبيقات ذات مستويات الهرمونات المستقرة مثل الإدارة عبر المهبل أو مكملات استراديول عبر الجلد. يمكن أيضًا أخذ جرعات منخفضة من هرمون الاستروجين في الاعتبار لهؤلاء المرضى. ومع ذلك، فإن البيانات المتاحة حتى الآن لا تزال غير كافية لتقديم بيانات موثوقة حول الفعالية والتحمل. على الرغم من أن العلاج الأحادي بالبروجستين له أكثر المخاطر خطورة على الأوعية الدموية، إلا أنه من الممكن ملاحظة آثار جانبية مثل النزيف الاختراقي.
وبشكل عام، تظهر الدراسات أن العلاج بالإستروجين هو العلاج الذي من المرجح أن يكون فعالاً ومقبولاً. ستكون الدراسات حول فعالية ومدى تحمل الإستروجين الطبيعي مهمة أيضًا في المستقبل. من المحتمل أن تكون الفترة القصيرة الخالية من الهرمونات أكثر فاعلية في منع انخفاض هرمون الاستروجين الذي قد يؤدي إلى نوبة الصداع النصفي. ومع ذلك، هناك حاجة إلى مزيد من الدراسات الخاضعة للرقابة في المستقبل حتى نتمكن من تقديم بيانات موثوقة هنا.
التوصيات التوجيهية الحالية للوقاية من الصداع النصفي الحيض
توصي الإرشادات الحالية الصادرة عن الجمعية الألمانية لطب الأعصاب (DGN) بالتعاون مع الجمعية الألمانية للصداع النصفي والصداع [63] اعتبارًا من عام 2022 باستخدام مضادات الالتهاب غير الستيروئيدية نابروكسين طويلة المفعول (نصف عمر 12-15 ساعة) أو تريبتان بنصف عمر طويل. الحياة للوقاية على المدى القصير من الصداع النصفي الحيض. يجب إعطاء المكونات النشطة قبل يومين من بداية الدورة الشهرية المتوقعة لمدة 5-6 أيام. علاوة على ذلك، يمكن اعتبار الإدارة المستمرة لوسائل منع الحمل المركبة عن طريق الفم بمثابة إجراء وقائي. ويمكن أيضًا النظر في استخدام عقار ديسوجيستريل للوقاية من الصداع النصفي الناتج عن الدورة الشهرية.
هناك دراسات مضبوطة بالعلاج الوهمي حول استخدام فروفاتريبتان 2.5 ملغ 1x أو 2x أو 3x يوميًا، وzolmitriptan 2.5 mg 2x أو 3x يوميًا، وnaratriptan 2x يوميًا 1 مجم أو 2.5 مجم ونابروكسين 2 × 550 مجم يوميًا من قبل. يجب أن تتم الإدارة قبل يومين من البداية المتوقعة لنوبة الصداع النصفي في فترة الحيض لمدة 6-7 أيام. يعتبر خطر الإصابة بصداع الإفراط في استخدام الدواء عند استخدام النابروكسين أو التريبتان للوقاية على المدى القصير من الصداع النصفي الحيضي منخفضًا إذا تم استخدام القليل من الأدوية الحادة.
لا توصي الإرشادات الحالية بإعطاء هرمون الاستروجين عن طريق الجلد. والسبب هو تأخر ظهور نوبة الصداع النصفي بعد التوقف عن تناول هلام الاستروجين. لا ينبغي النظر في مكملات الاستروجين عن طريق الجلد إلا إذا كانت التدابير الوقائية الأخرى غير فعالة. الشرط الأساسي لهذا الإجراء هو دورة منتظمة لتحديد وقت التطبيق. لا يُنصح باستخدام مكملات هرمون الاستروجين الإضافية عن طريق الجلد في الفترة الخالية من حبوب منع الحمل للوقاية من الصداع النصفي الناتج عن الصداع النصفي الناتج عن الدورة الشهرية بسبب نقص البيانات.
وفقًا للمبادئ التوجيهية الحالية، يمكن اعتبار الإدارة المستمرة لوسائل منع الحمل المركبة عن طريق الفم بمثابة إجراء وقائي. الهدف هو تقليل عدد الدورات ونوبات الصداع النصفي التي تسببها. يعتبر الاستخدام المستمر لمدة تصل إلى عامين آمنًا. تشير المبادئ التوجيهية إلى أن هذا العلاج الوقائي للصداع ونوبات الصداع النصفي خارج فترة الدورة الشهرية لم يتم فحصه حتى الآن إلا في دراسات مفتوحة وغير خاضعة للرقابة. بما أن موانع الحمل الفموية المشتركة يمكن أن تزيد بشكل كبير من خطر الإصابة بالسكتة الدماغية والصداع النصفي مع الهالة بحد ذاتها هي عامل خطر للسكتات الدماغية، يجب أن يؤخذ ملف المخاطر القلبية الوعائية لكل مريض في الاعتبار على حدة. وفقًا للمبادئ التوجيهية، فإن الاستخدام المستمر لموانع الحمل الفموية المركبة هو الأقل إثارة للقلق لدى المرضى الذين يعانون من الصداع النصفي فقط دون هالة وبدون عوامل خطر القلب والأوعية الدموية الأخرى. وبخلاف ذلك، يجب تحديد المؤشرات بدقة، ويجب إبلاغ المريض وفقًا لذلك ويجب تحديد الإجراء على أساس كل حالة على حدة. ينبغي عمومًا تفضيل موانع الحمل الفموية المركبة ذات المحتوى المنخفض من هرمون الاستروجين. موانع لاستخدام وسائل منع الحمل عن طريق الفم مجتمعة هو الصداع النصفي النشط للغاية مع هالة في المرضى الذين يعانون من زيادة خطر الأوعية الدموية.
ويجب أيضًا ضمان وسائل منع الحمل المناسبة باستخدام العلاجات الوقائية المختلفة للصداع النصفي. وينطبق هذا بشكل خاص على العلاج بالأجسام المضادة وحيدة النسيلة ضد CGRP أو مستقبل CGRP وتوكسين البوتولينوم والفلوناريزين والتوبيراميت والفالبروات.
موانع الحمل الهرمونية وخطر السكتة الدماغية والصداع النصفي في الممارسة العملية
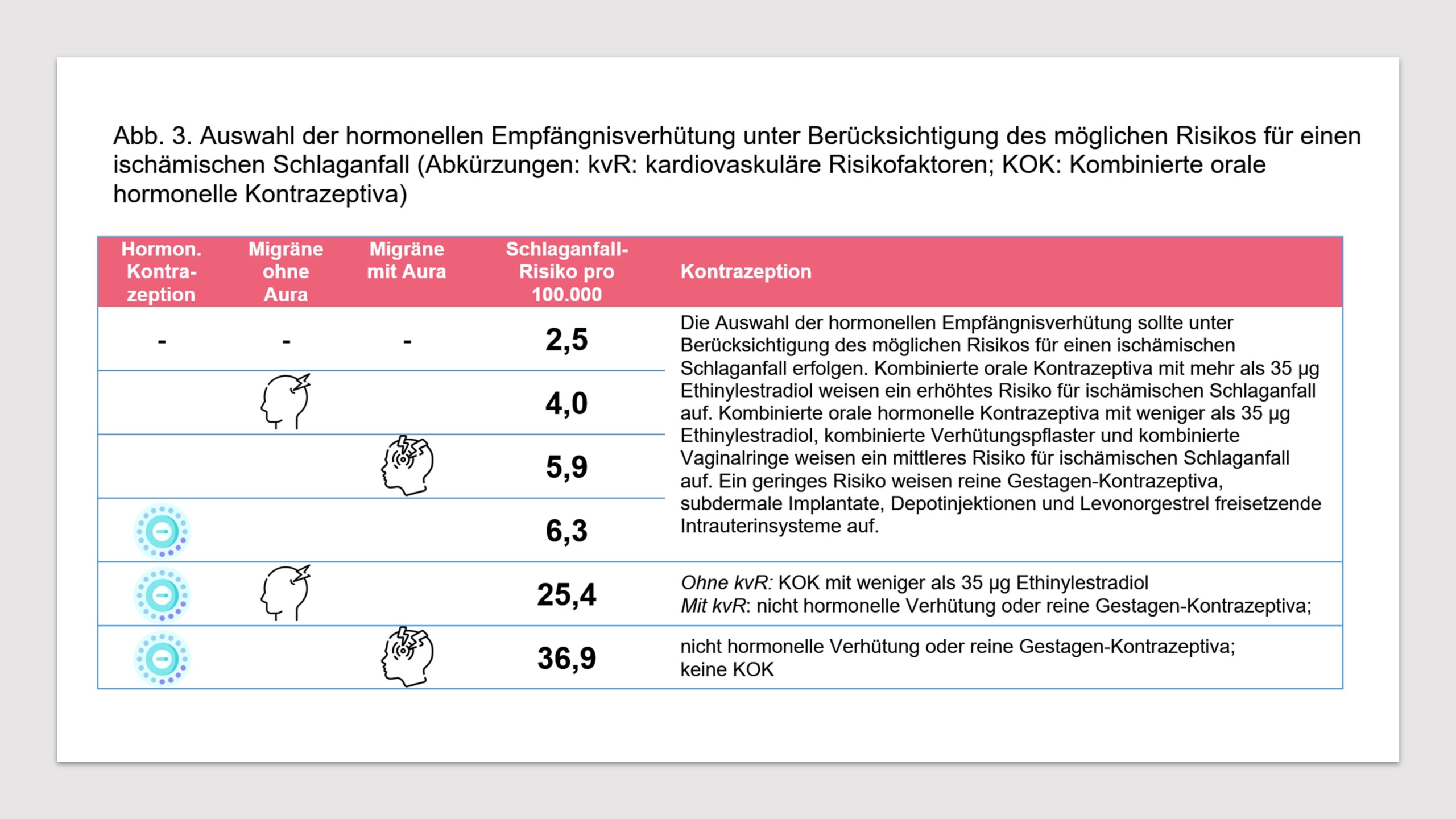
الصداع النصفي هو عامل خطر للسكتة الدماغية وغيرها من الأحداث الوعائية. هناك أدلة واسعة النطاق على أن زيادة خطر الإصابة بالسكتة الدماغية يرتبط بكل من الصداع النصفي بدون هالة والصداع النصفي مع هالة [4، 30، 32، 33، 58-60]. نظرًا لأنه يمكن أيضًا زيادة خطر الإصابة بالسكتة الدماغية عند استخدام موانع الحمل الهرمونية المركبة [4، 32، 61]، فإن السؤال ذو الصلة هو ما إذا كان الوجود المتزامن للصداع النصفي واستخدام موانع الحمل الهرمونية المركبة يمكن أن يزيد من خطر الإصابة بالسكتة الدماغية. قام الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH) بتحليل هذا السؤال في بيان إجماعي [33]. يبلغ الخطر المطلق للإصابة بالسكتة الدماغية لدى النساء اللاتي لا يستخدمن وسائل منع الحمل الهرمونية 2.5/100000 سنويًا. نفس الخطر بالنسبة للنساء اللاتي يستخدمن وسائل منع الحمل الهرمونية هو 6.3/100000. إذا كانت النساء يعانين من الصداع النصفي مع هالة، فإن خطر الإصابة بسكتة دماغية إقفارية دون تناول وسائل منع الحمل الهرمونية هو 5.9 لكل 100.000 سنويًا. إن خطر الإصابة بسكتة دماغية إقفارية إذا كنت تعاني من الصداع النصفي المصحوب بهالة وتستخدم وسائل منع الحمل الهرمونية هو 36.9/100000 سنويًا. وبالنظر إلى النساء اللاتي يعانين من الصداع النصفي بدون هالة، فإن خطر الإصابة بالسكتة الإقفارية هو 4.0/100.000 سنويًا. إذا تم استخدام وسائل منع الحمل الهرمونية في هذه المجموعة، فإن الخطر يصل إلى 25.4/100000 سنوياً (انظر الشكل 3).
يستمد الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH) إجماع الخبراء التالي من البيانات [33]:
- إذا كانت المرأة تسعى جاهدة من أجل وسائل منع الحمل الهرمونية ، يوصى بفحص سريري لتحليل ما إذا كان هناك صداع نصفي مع الصداع النصفي بدون هالة. بالإضافة إلى ذلك ، ينبغي تحديد تردد الصداع النصفي (أيام الصداع في الشهر) وتحديد عوامل الخطر الوعائية قبل وصفة طبية من وسائل منع الحمل الهرمونية المشتركة.
- يُنصح النساء اللاتي يرغبن في استخدام وسائل منع الحمل الهرمونية باستخدام أداة خاصة لتشخيص الصداع النصفي وأنواعه الفرعية. ويمكن استخدام الاستبيانات أو الخيارات الرقمية مثل تطبيق الصداع النصفي (يمكن تنزيله مجانًا من متاجر التطبيقات تحت هذا الاسم) لهذا الغرض.
- يجب أن يتم اختيار وسائل منع الحمل الهرمونية مع الأخذ بعين الاعتبار المخاطر المحتملة للسكتة الدماغية. تزيد موانع الحمل الفموية المركبة التي تحتوي على أكثر من 35 ميكروغرام من إيثينيل استراديول من خطر الإصابة بالسكتة الإقفارية. موانع الحمل الهرمونية الفموية المركبة التي تحتوي على أقل من 35 ميكروغرام من إيثينيل استراديول، ولصقات منع الحمل المركبة، والحلقات المهبلية المركبة لها خطر متوسط للإصابة بالسكتة الإقفارية. تشكل وسائل منع الحمل التي تحتوي على البروجستين فقط، والغرسات تحت الجلد، والحقن المستودعية، والأنظمة داخل الرحم التي تطلق الليفونورجيستريل خطرًا منخفضًا.
- يُنصح النساء المصابات بالصداع النصفي المصحوب بهالة ويبحثن عن وسائل منع الحمل الهرمونية بعدم وصف وسائل منع الحمل الهرمونية المركبة.
- بالنسبة للنساء اللاتي يعانين من الصداع النصفي مع هالة ويبحثن عن وسائل منع الحمل، يوصى باستخدام وسائل منع الحمل غير الهرمونية (الواقي الذكري، الأجهزة الرحمية المحتوية على النحاس، أو وسائل منع الحمل التي تحتوي على البروجستيرون فقط) كخيار مفضل. في حالة حدوث الصداع النصفي مع هالة ويتم بالفعل استخدام وسائل منع الحمل الهرمونية المركبة لمنع الحمل، يوصى بالتحول إلى وسائل منع الحمل غير الهرمونية أو وسائل منع الحمل التي تحتوي على البروجستين فقط.
- في النساء اللاتي يعانين من الصداع النصفي بدون هالة والذين يرغبون في استخدام وسائل منع الحمل الهرمونية، ولكن لديهم عوامل خطر إضافية (التدخين، ارتفاع ضغط الدم الشرياني، السمنة، أمراض القلب والأوعية الدموية، تجلط الأوردة العميقة أو الانسداد الرئوي في الماضي)، وسائل منع الحمل غير الهرمونية أو البروجستيرون. - يوصى باستخدام وسائل منع الحمل فقط كخيار مفضل.
- في النساء اللاتي يعانين من الصداع النصفي بدون هالة ويستخدمن وسائل منع الحمل الهرمونية وليس لديهن عوامل خطر إضافية، يوصى باستخدام وسائل منع الحمل الهرمونية المركبة بجرعة أقل من 35 ميكروغرام من إيثينيل استراديول لمنع الحمل. وفي الوقت نفسه، ينبغي مراقبة وتيرة وخصائص الصداع النصفي.
- إذا كانت النساء يعانين من الصداع النصفي مع هالة أو الصداع النصفي بدون هالة ويحتاجن إلى علاج هرموني بسبب متلازمة المبيض المتعدد الكيسات أو التهاب بطانة الرحم، فمن المستحسن استخدام العلاج الهرموني مع البروجستين النقي أو وسائل منع الحمل الهرمونية المركبة وفقا للاعتبارات السريرية.
- إذا بدأت النساء في منع الحمل باستخدام وسائل منع الحمل الهرمونية المدمجة وتطور لديهن صداع نصفي جديد مع هالة أو عندما يحدث الصداع النصفي بدون هالة لأول مرة على مقربة من بداية تناول وسائل منع الحمل الهرمونية، فيجب التحول إلى وسائل منع الحمل غير الهرمونية أو البروجستين. يوصى فقط - يوصى باستخدام وسائل منع الحمل.
- إذا كانت النساء اللاتي يعانين من الصداع النصفي مع أو بدون هالة بحاجة إلى وسائل منع الحمل الطارئة، يوصى باستخدام الليفونورجيستريل 1.5 ملغ عن طريق الفم، أو أسيتات وليبريستال 30 ملغ عن طريق الفم أو جهاز داخل الرحم يحتوي على النحاس.
- إذا بدأت النساء المصابات بالصداع النصفي مع أو بدون هالة في تناول وسائل منع الحمل الهرمونية، فإن اختبارات محددة مثل فحص أهبة التخثر أو فحص الثقبة البيضوية الواضحة أو اختبارات التصوير ليست ذات صلة بقرار استخدام وسائل منع الحمل الهرمونية ما لم يتطلب التاريخ الطبي أو النتائج تحقيقات مناسبة بسبب عوامل محددة. معلومة.
- بالنسبة للنساء اللاتي يعانين من صداع غير الصداع النصفي ويبحثن عن وسائل منع الحمل الهرمونية، يمكن استخدام أي وسيلة منع حمل هرمونية بجرعة منخفضة.
بشكل عام، الأدلة على العلاقة بين السكتة الدماغية واستخدام وسائل منع الحمل الهرمونية محدودة. في الأساس، تتوفر فقط الدراسات الرصدية غير المنضبطة. يجب إجراء المزيد من الدراسات في المستقبل لتحديد المخاطر المحتملة لوسائل منع الحمل الهرمونية لدى النساء المصابات بالصداع النصفي. ومع ذلك، تظهر البيانات حتى الآن زيادة خطر الإصابة بالسكتة الدماغية المرتبطة باستخدام وسائل منع الحمل الهرمونية لدى النساء المصابات بالصداع النصفي. في هذه الحالة، من الضروري إيلاء اهتمام خاص لجوانب السلامة أثناء الاستخدام. على الرغم من أن خطر الإصابة بالسكتة الدماغية ليس مرتفعًا جدًا، إلا أن السكتة الدماغية يمكن أن يكون لها عواقب وخيمة على الأفراد وأسرهم. لهذه الأسباب، ينبغي استخدام وسائل منع الحمل البديلة إذا كان هناك خطر متزايد مماثل.
الأدب
- لجنة تصنيف الصداع التابعة لجمعية الصداع الدولية (IHS)، التصنيف الدولي لاضطرابات الصداع ICHD-3، الطبعة الثالثة. الصداع النصفي، 2018. 38 (1): ص. 1-211.
- معايير التصنيف والتشخيص لاضطرابات الصداع والألم العصبي القحفي وآلام الوجه. لجنة تصنيف الصداع التابعة لجمعية الصداع الدولية. الصداع النصفي، 1988. 8 ملحق 7 : ص. 1-96.
- التصنيف الدولي لاضطرابات الصداع: الطبعة الثانية. الصداع النصفي، 2004. 24 ملحق 1 : ص. 9-160.
- نابي، ري، وآخرون، دور هرمون الاستروجين في الصداع النصفي الحيض. الخلايا، 2022. 11 (8).
- راسل، MB، علم الوراثة من الصداع النصفي الحيض: الأدلة الوبائية. ممثل صداع الألم، 2010. 14 (5): ص. 385-8.
- Somerville، BW، دور انسحاب استراديول في مسببات الصداع النصفي الحيض. علم الأعصاب، 1972. 22 (4): ص. 355-65.
- بافلوفيتش، جي إم، وآخرون، الهرمونات الجنسية لدى النساء المصابات بالصداع النصفي وبدونه. علم الأعصاب، 2016. 87 (1): ص. 49.
- كورنيل، كاليفورنيا، جي إف بول، وجي. بالتزارت، الأهمية الوظيفية للتنظيم السريع لعمل هرمون الاستروجين في الدماغ: من أين يأتي هرمون الاستروجين؟ دقة الدماغ، 2006. 1126 (1): ص. 2-26.
- Boese، AC، et al.، الاختلافات بين الجنسين في فسيولوجيا الأوعية الدموية والفيزيولوجيا المرضية: إشارات الاستروجين والأندروجين في الصحة والمرض. Am J Physiol Heart Circ Physiol، 2017. 313 (3): ص. H524-h545.
- رودريغيز-أسيفيدو، AJ، وآخرون، إلى أن المتغيرات الجينية في جينات SYNE1 وTNF مرتبطة بالصداع النصفي الحيضي. J ألم الصداع، 2014. 15 (1): ص. 62.
- Vetvik، KG و EA MacGregor، الصداع النصفي الحيض: اضطراب متميز يحتاج إلى مزيد من الاعتراف. لانسيت نيورول، 2021. 20 (4): ص. 304-315.
- Shughrue، PJ and I. Merchenthaler، الاستروجين هو أكثر من مجرد "هرمون جنسي": مواقع جديدة لعمل الاستروجين في الحصين والقشرة الدماغية. الغدد الصم العصبية الأمامية، 2000. 21 (1): ص. 95-101.
- Facchinetti، F.، وآخرون، تقييم الغدد الصم العصبية للنشاط الأفيوني المركزي في اضطرابات الصداع الأولية. الألم، 1988. 34 (1): ص. 29-33.
- تاسوريلي، سي، وآخرون، التغيرات في عتبة منعكس انثناء مسبب للألم عبر الدورة الشهرية لدى النساء الأصحاء. سايكوسوم ميد، 2002. 64 (4): ص. 621-6.
- كراوس، دي إن، وآخرون، التأثيرات الهرمونية في الصداع النصفي – تفاعلات هرمون الاستروجين والأوكسيتوسين وCGRP. نات ريف نيورول، 2021. 17 (10): ص. 621-633.
- De Icco، R.، et al.، تعديل عتبة مسبب للألم عن طريق وسائل منع الحمل الهرمونية المدمجة لدى النساء المصابات بنوبات الصداع النصفي لانسحاب الإستروجين: دراسة تجريبية. J ألم الصداع، 2016. 17 (1): ص. 70.
- Warfvinge، K.، وآخرون، مستقبلات هرمون الاستروجين α و β و GPER في الجهاز العصبي المركزي والجهاز الثلاثي التوائم – الجوانب الجزيئية والوظيفية. J ألم الصداع، 2020. 21 (1): ص. 131.
- كيتازاوا، ت، وآخرون، آلية غير جينومية لتثبيط 17 بيتا-أوستراديول للتقلص في العضلات الملساء الوعائية للثدييات. J Physiol، 1997. 499 (جزء 2) (جزء 2): ص. 497-511.
- سومجين، جي جي، آليات انتشار الاكتئاب ونقص التأكسج المنتشر لإزالة الاستقطاب الشبيه بالاكتئاب. القس فيزيول، 2001. 81 (3): ص. 1065-96.
- Edvinsson، L.، وآخرون، CGRP كهدف لعلاجات الصداع النصفي الجديدة - ترجمة ناجحة من مقاعد البدلاء إلى العيادة. نات ريف نيورول، 2018. 14 (6): ص. 338-350.
- Knight، YE، L. Edvinsson، و PJ Goadsby، 4991W93 يمنع إطلاق الببتيد المرتبط بجين الكالسيتونين في القطة ولكن فقط عند الجرعات التي تحتوي على نشاط ناهض مستقبلات 5HT (1B / 1D)؟ علم الأدوية العصبية، 2001. 40 (4): ص. 520-5.
- أشينا، م.، الصداع النصفي. N Engl J Med، 2020. 383 (19): ص. 1866-1876.
- فوربس، آر بي، إم. ماكارون، وسي آر كاردويل، الفعالية والتأثيرات السياقية (الدواء الوهمي) للأجسام المضادة لـ CGRP للصداع النصفي: مراجعة منهجية وتحليل تلوي. الصداع، 2020. ص60 (8): ص. 1542-1557.
- Drellia، K.، et al.، الأجسام المضادة وحيدة النسيلة المضادة لـ CGRP للوقاية من الصداع النصفي: مراجعة منهجية واحتمال المساعدة في التحليل أو الإضرار به. صداع، 2021. 41 (7): ص. 851-864.
- فالديمارسون، س.، وآخرون، التأثير الهرموني على الببتيد المرتبط بجينات الكالسيتونين في الإنسان: آثار اختلاف الجنس وحبوب منع الحمل. Scand J Clin Lab Invest، 1990. 50 (4): ص. 385-8.
- Gupta، P.، et al.، آثار حالة انقطاع الطمث على تعميم الببتيد والأديبوكينات المرتبطة بجينات الكالسيتونين: الآثار المترتبة على مقاومة الأنسولين ومخاطر القلب والأوعية الدموية. سن اليأس، 2008. 11 (5): ص. 364-72.
- Aggarwal، M.، V. Puri، and S. Puri، تأثيرات هرمون الاستروجين على نظام هرمون السيروتونين والببتيد المرتبط بجينات الكالسيتونين في العقد الثلاثي التوائم للفئران. آن نيوروسي، 2012. 19 (4): ص. 151-7.
- Cetinkaya، A.، وآخرون، آثار هرمون الاستروجين والبروجستيرون على الببتيدات العصبية الالتهابية العصبية: الآثار المترتبة على الاختلافات بين الجنسين في الصداع النصفي. إكسب برين ريس، 2020. 238 (11): ص. 2625-2639.
- ياماناكا، ج.، وآخرون، دور الالتهاب العصبي وقابلية تغير حاجز الدم في الدماغ في الصداع النصفي. Int J Mol Sci، 2021. 22 (16).
- Cupini، LM، I. Corbelli، and P. Sarchelli، الصداع النصفي الحيضي: ما هو وهل يهم؟ ج نيورول، 2021. 268 (7): ص. 2355-2363.
- ماكجريجور، EA، وآخرون، حدوث الصداع النصفي بالنسبة لمراحل الدورة الشهرية لارتفاع وانخفاض هرمون الاستروجين. علم الأعصاب، 2006. 67 (12): ص. 2154-8.
- ساكو، إس، وآخرون، تأثير هرمون الاستروجين والمركبات بروجستيرونية المفعول الخارجية على مسار الصداع النصفي أثناء سن الإنجاب: بيان إجماعي من قبل الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESCRH). J ألم الصداع، 2018. 19 (1): ص. 76.
- ساكو، إس، وآخرون، موانع الحمل الهرمونية وخطر الإصابة بالسكتة الإقفارية لدى النساء المصابات بالصداع النصفي: بيان إجماعي من الاتحاد الأوروبي للصداع (EHF) والجمعية الأوروبية لمنع الحمل والصحة الإنجابية (ESC). J ألم الصداع، 2017. 18 (1): ص. 108.
- Merki-Feld، GS، et al.، تحسين الصداع النصفي مع التغيير من وسائل منع الحمل الهرمونية المركبة إلى وسائل منع الحمل التي تحتوي على البروجستين فقط مع الديسوجيستريل: ما مدى قوة تأثير إبعاد النساء عن وسائل منع الحمل المركبة؟ J Obstet Gynaecol، 2017. 37 (3): ص. 338-341.
- Morotti، M.، et al.، حبوب منع الحمل التي تحتوي على البروجستيرون فقط مقارنة مع وسائل منع الحمل عن طريق الفم مجتمعة في علاج أعراض الألم الناجمة عن التهاب بطانة الرحم في المرضى الذين يعانون من الصداع النصفي دون هالة. يورو J أوبستيت جينكول ريبرود بيول، 2014. 179 : ص. 63-8.
- Morotti، M.، et al.، وسائل منع الحمل البروجستين فقط مقارنة مع وسائل منع الحمل الفموية المشتركة الموسعة لدى النساء المصابات بالصداع النصفي بدون هالة: دراسة تجريبية بأثر رجعي. يورو J أوبستيت جينكول ريبرود بيول، 2014. 183 : ص. 178-82.
- Nappi، RE، et al.، آثار وسائل منع الحمل عن طريق الفم الخالية من هرمون الاستروجين والتي تحتوي على الديسوجيستريل لدى النساء المصابات بالصداع النصفي مع الهالة: دراسة تجريبية مستقبلية تعتمد على المذكرات. منع الحمل، 2011. 83 (3): ص. 223-8.
- Coffee، AL، et al.، الدورة الممتدة تجمع بين وسائل منع الحمل عن طريق الفم والفروفاتريبتان الوقائي خلال فترة خالية من الهرمونات لدى النساء المصابات بالصداع النصفي المرتبط بالدورة الشهرية. J صحة المرأة (لارشمت)، 2014. 23 (4): ص. 310-7.
- كالهون، آه، علاج وقائي محدد جديد للصداع النصفي المرتبط بالدورة الشهرية. جنوب ميد ج، 2004. 97 (9): ص. 819-22.
- Macgregor، EA و A. Hackshaw، الوقاية من الصداع النصفي في الفترة الخالية من حبوب منع الحمل عن طريق الفم مجتمعة: دراسة تجريبية مزدوجة التعمية، يتم التحكم فيها بالعلاج الوهمي باستخدام مكملات الاستروجين الطبيعية. J Fam Plann Reprod Health Care، 2002. 28 (1): ص. 27-31.
- LaGuardia، KD، وآخرون، قمع صداع انسحاب هرمون الاستروجين مع وسائل منع الحمل الموسعة عبر الجلد. فيرتيل ستريل، 2005. 83 (6): ص. 1875-7.
- Calhoun، A.، S. Ford، and A. Pruitt، تأثير وسائل منع الحمل الحلقية المهبلية ذات الدورة الممتدة على هالة الصداع النصفي: سلسلة حالات بأثر رجعي. الصداع، 2012. 52 (8): ص. 1246-53.
- de Lignières، B.، وآخرون، الوقاية من الصداع النصفي الحيضي عن طريق استراديول عن طريق الجلد. بر ميد جي (كلين ريس إد)، 1986. 293 (6561): ص. 1540.
- Dennerstein، L.، et al.، الصداع النصفي أثناء الدورة الشهرية: تجربة مزدوجة التعمية للاستراديول عن طريق الجلد. جينكول إندوكرينول، 1988. 2 (2): ص. 113-20.
- ماكجريجور، EA، وآخرون، الوقاية من نوبات الصداع النصفي أثناء الدورة الشهرية: دراسة متقاطعة مزدوجة التعمية يتم التحكم فيها بالعلاج الوهمي. علم الأعصاب، 2006. 67 (12): ص. 2159-63.
- Martin، V.، et al.، استئصال المبيض الطبي مع أو بدون العلاج الإضافي بالإستروجين في الوقاية من الصداع النصفي. الصداع، 2003. 43 (4): ص. 309-21.
- ماجوس، AL، KJ Zilkha، وJW Studd، علاج الصداع النصفي الحيض عن طريق زراعة استراديول. J Neurol Neurosurg الطب النفسي، 1983. 46 (11): ص. 1044-6.
- Murray، SC and KN Muse، العلاج الفعال للصداع النصفي الحاد في الدورة الشهرية باستخدام ناهض هرمون إفراز الغدد التناسلية والعلاج "الإضافة". فيرتيل ستريل، 1997. 67 (2): ص. 390-3.
- فيرانتي، ف.، وآخرون، الاستروجين النباتي في الوقاية من الصداع النصفي الحيضي. كلين نيوروفارماكول، 2004. 27 (3): ص. 137-40.
- Burke، BE، RD Olson، and BJ Cusack، تجربة عشوائية محكومة للاستروجين النباتي في العلاج الوقائي للصداع النصفي الحيضي. بيوميد فارماكوثر، 2002. 56 (6): ص. 283-8.
- Eikermann-Haerter، K.، et al.، قمع منشط الذكورة لانتشار الاكتئاب في الفئران المتحولة من النوع الأول من الصداع النصفي الفالجي العائلي. آن نيورول، 2009. 66 (4): ص. 564-8.
- Nappi، RE، K. Wawra، and S. Schmitt، اضطراب الرغبة الجنسية الناقص النشاط لدى النساء بعد انقطاع الطمث. جينكول إندوكرينول، 2006. 22 (6): ص. 318-23.
- ماكجريجور، EA، الصداع النصفي أثناء الدورة الشهرية وانقطاع الطمث: مراجعة سردية. ماتوريتاس، 2020. 142 : ص. 24-30.
- Schoretsanitis، G.، وآخرون، التفاعلات الدوائية بين الأدوية العقلية ووسائل منع الحمل عن طريق الفم. رأي الخبراء في دواء ميتاب توكسيكول، 2022. 18 (6): ص. 395-411.
- لازورويتز، أ.، وآخرون، تأثير التوبيرامات على تركيزات الإيتونوجيستريل في الدم بين مستخدمي وسائل منع الحمل المزروعة. أوبستيت جينيكول، 2022. 139 (4): ص. 579-587.
- أورنيلو، ر.، وآخرون، صداع الدورة الشهرية لدى النساء المصابات بالصداع النصفي المزمن المعالجات بإرينوماب: سلسلة حالات رصدية. علوم الدماغ، 2021. 11 (3).
- بافلوفيتش، جي إم، وآخرون، فعالية وسلامة إرينوماب لدى النساء اللاتي لديهن تاريخ من الصداع النصفي الحيضي. J ألم الصداع، 2020. 21 (1): ص. 95.
- Adewuyi، EO، وآخرون، الآليات الوراثية الجزيئية المشتركة تكمن وراء التهاب بطانة الرحم والاعتلال المشترك للصداع النصفي. الجينات (بازل)، 2020. 11 (3).
- صديق، SE، وآخرون، خطر الإصابة بالسكتة الدماغية لدى النساء النصفيات، ارتباط خفي: مراجعة منهجية. كيوريوس، 2022. 14 (7): ص. e27103.
- Siao، WZ، وآخرون، خطر الإصابة بأمراض الشريان المحيطي والسكتة الدماغية لدى المصابين بالصداع النصفي مع أو بدون هالة: دراسة أترابية قائمة على السكان على مستوى البلاد. Int J Med Sci، 2022. 19 (7): ص. 1163-1172.
- Champaloux، SW، وآخرون، استخدام وسائل منع الحمل الهرمونية المركبة بين النساء المصابات بالصداع النصفي وخطر الإصابة بالسكتة الدماغية. آم جي أوبستيت جينيكول، 2017. 216 (5): ص. 489.e1-489.e7.
- وسائل منع الحمل الهرمونية المبادئ التوجيهية لـ DGGG وSGGG وOEGGG (المستوى S3، سجل AWMF رقم 015/015، نوفمبر 2019). https://register.awmf.org/de/leitlinien/detail/015-015 .
- Diener، H.-C.، وآخرون، علاج نوبات الصداع النصفي والوقاية من الصداع النصفي، إرشادات S1، 2022، DGN وDMKG ، في إرشادات التشخيص والعلاج في علم الأعصاب ، DGfN (ed.)، محرر. 2022: عبر الإنترنت: www.dgn.org/leitlinien .










اترك تعليقا