Remarque : Les explications suivantes décrivent les théories scientifiques relatives au développement des céphalées en grappe. Elles sont rédigées en termes scientifiques.
Site d'origine de la céphalée en grappe
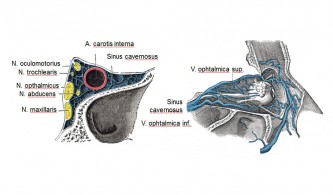
L'une des principales caractéristiques des céphalées en grappe est leur localisation derrière et autour de l'œil . Ces céphalées peuvent également survenir chez des personnes une énucléation (ablation du même côté que la douleur) peu probable douleur de l'œil lui-même . De ce fait, il est probable que la céphalée prenne naissance dans les structures situées autour ou derrière l'œil . Pour déterminer les structures jouant un rôle crucial dans le développement des céphalées en grappe, il est important de noter que ces céphalées peuvent également survenir dans le cadre maladies symptomatiques . Parmi ces entités cliniques bien définies, on peut citer les méningiomes cervicaux supérieurs , les méningiomes parasellaires , les malformations artérioveineuses importantes dans diverses structures cérébrales ipsilatérales , les kystes ethmoïdaux au niveau du clivus et des citernes suprasellaires , les adénomes hypophysaires , les calcifications au niveau du troisième ventricule, les anévrismes ipsilatéraux et les anévrismes de l'artère communicante antérieure . Toutes ces structures présentent un rapport avec la ligne médiane au niveau du sinus caverneux . Il est donc raisonnable de supposer que le sinus caverneux est la structure anatomique particulièrement impliquée dans la genèse des céphalées en grappe.
au cours de l'évolution spontanée d'une céphalée en grappe. Les IRM effectuées pendant une crise ont montré une augmentation du contraste au niveau du sinus caverneux , indiquant un processus inflammatoire survenant dans ce sinus durant la crise. De plus, des signes d'inflammation ont été détectés dans le liquide céphalo-rachidien et le sang périphérique pendant l'épisode de céphalée en grappe . La phlébographie a révélé des signes de vascularite veineuse au niveau du sinus caverneux et de la veine oculomotrice supérieure pendant la période de crises. Fait intéressant, ces anomalies ont complètement régressé pendant la rémission . Ces investigations suggèrent que le système veineux et le sinus caverneux jouent un rôle important dans le développement de la douleur associée à la céphalée en grappe.
L' innervation parasympathique est assurée par le nerf pétreux profond et les branches orbitaires issues du ganglion sphénopalatin , ainsi que par d'autres microganglions. Les fibres parasympathiques traversent la fissure supra-orbitaire au niveau du sinus caverneux . Les fibres sensitives innervant l'orbite proviennent du nerf ophtalmique et passent également, en partie, au niveau du sinus caverneux . Certaines de ces fibres vascularisent l'artère basilaire et, à ce titre, longent le nerf abducens sur une portion de leur trajet. Le nerf grand pétreux superficiel innerve également l' artère carotide interne par des fibres sensitives. Le sinus caverneux est innervé par des fibres des trijumeau et facial . Les veines et les sinus duraux sont innervés par des fibres nociceptives issues du nerf tentoriel . Les fibres sensitives, sympathiques et parasympathiques forment un plexus au niveau du sinus caverneux . Des mécanorécepteurs supplémentaires sont situés le long du trajet de l'artère carotide interne, dans le canal carotidien.
L' origine des céphalées en grappe peut être localisée du sinus caverneux grâce aux structures anatomiques et aux observations mentionnées précédemment L'angiographie carotidienne révèle une dilatation , ou une obstruction du passage lors de la phlébographie orbitaire pendant les crises. Ces modifications, en particulier la dilatation du sinus caverneux, sont observées du côté de la céphalée. De plus, des dilatations vasculaires peuvent être observées pendant les crises au niveau de l' artère ophtalmique , de l' artère cérébrale antérieure et de l' artère cérébrale moyenne
Une dilatation vasculaire des ophtalmique et cérébrale antérieure également été entre les crises de céphalée en grappe . De ce fait, le lien de causalité direct entre cette dilatation et l'apparition de la douleur . Toutefois, indépendamment de ce lien, le caractère ipsilatéral de la dilatation suggère une corrélation entre les phases de dilatation et les épisodes de céphalée.
Les examens phlébographiques révèlent des signes de phlébite au niveau de la veine ophtalmique supérieure et du sinus caverneux des observations similaires également faites dans le syndrome de Tolosa-Hunt , où une inflammation granulomateuse des structures correspondantes est suspectée. Ces deux affections peuvent être traitées très efficacement par une corticothérapie anti -inflammatoire . On ignore encore totalement pourquoi une inflammation du sinus caverneux et des veines environnantes survient lors d'une crise de céphalée en grappe.
On peut supposer que le rétrécissement des voies aériennes nasales et sinusales chez les patients souffrant de céphalées en grappe pourrait entraîner une altérée des cellules ethmoïdales , favorisant ainsi une infection ipsilatérale. La propagation subséquente de l'inflammation au sinus caverneux ipsilatéral hypothèse possible pour la pathogenèse des céphalées en grappe. Cependant, aucune preuve ne vient étayer cette hypothèse. Ces considérations sont renforcées par l'incidence accrue chez les fumeurs. De plus, les crises surviennent généralement pendant les saisons où le risque d'infections des voies respiratoires supérieures est plus élevé.
Études de neuroimagerie et de morphométrie
Les considérations physiopathologiques relatives au développement des céphalées en grappe doivent prendre en compte le moment d'apparition, le regroupement temporaire des crises, leur localisation et l'implication des systèmes sympathique et parasympathique. Initialement, le développement des céphalées en grappe était expliqué par des variations du diamètre vasculaire. Ceci a également permis de mieux comprendre les effets des substances vasoconstrictrices et le déclenchement des crises par des vasodilatateurs tels que la nitroglycérine et l'histamine.
La tomographie par émission de positons (TEP) permet d'examiner les variations du débit sanguin cérébral régional. Les examens TEP à haute résolution permettent de détecter même de subtiles variations de ce débit, au repos et lors de certains processus d'activation cérébrale. Les crises de céphalée en grappe peuvent être induites expérimentalement par la nitroglycérine. Ces crises induites expérimentalement ne diffèrent pas des crises spontanées en ce qui concerne les principaux paramètres physiopathologiques. Les céphalées en grappe induites expérimentalement, tout comme les céphalées en grappe spontanées, peuvent être traitées efficacement par le sumatriptan.
Le groupe de recherche de May et al. (1998) a décrit une activation significative dans l'hypothalamus ipsilatéral pendant les céphalées en grappe aiguës chez un groupe de patients souffrant de céphalées en grappe, par rapport à la période sans céphalée.
- Aucune activation du tronc cérébral n'a été constatée chez les patients souffrant de céphalées en grappe, ce qui a permis de supposer une distinction avec d'éventuels processus physiopathologiques du tronc cérébral, comme dans le cas de la migraine.
- Ces résultats confirment également l'expérience clinique selon laquelle les médicaments utilisés pour traiter les céphalées en grappe ne sont pas efficaces pour prévenir les migraines, et vice versa.
- aucune activation du tronc cérébral n'a pu être détectée lors de la stimulation douloureuse expérimentale du front par la capsaïcine , et aucune activation hypothalamique lors de l'induction douloureuse expérimentale par la capsaïcine dans la région du front.
- Sur la base de ces résultats, il a été conclu que l'activation hypothalamique est un processus spécifique de la céphalée en grappe, associé au déclenchement ou au maintien de la douleur, et non une réponse secondaire à l'activation des nocicepteurs dans la zone de la première branche du nerf trijumeau.
- L'hypothalamus doit être stimulé au cours de la phase aiguë de la céphalée en grappe. Les rythmes circadiens et les cycles veille-sommeil sont censés activer les noyaux hypothalamiques, qui constituent le principal facteur d'activation.
Le concept de céphalées primaires postule que des modifications fonctionnelles sont à l'origine des maux de tête. On ne suppose pas de modifications structurelles du cerveau dans les céphalées primaires. Cependant, grâce à la morphométrie basée sur les voxels, une modification structurelle significative de la densité de la substance grise a été décrite par rapport aux sujets témoins sains. Ces modifications ont été observées aussi bien pendant qu'en dehors des crises. Les différences étaient localisées bilatéralement dans la région du diencéphale adjacente au troisième ventricule et rostrale à l'aqueduc de Sylvius. Cette région coïncide avec l'aire de l' hypothalamus postéro-inférieur . Des observations similaires ne sont pas retrouvées chez les patients migraineux. Ceci a conduit à l'hypothèse que des modifications structurelles pourraient être associées au processus pathologique des céphalées en grappe, tandis que des mécanismes purement fonctionnels joueraient un rôle dans la migraine.
D’après les résultats d’imagerie obtenus par TEP et IRMf avec analyses morphométriques voxel-based, les modifications vasculaires vasoconstrictrices et vasodilatatrices directes ne constituent plus l’élément central de la physiopathologie des céphalées en grappe. Des modifications fonctionnelles et structurelles du mésencéphale et du pont ont été postulées dans la migraine, tandis que des modifications correspondantes de la substance grise hypothalamique ont été suspectées dans les céphalées en grappe. Outre les mécanismes d’activation fonctionnelle, des modifications structurelles de la densité de la substance grise hypothalamique sont également envisagées.
À partir de ces observations, la stimulation cérébrale profonde (SCP) a été proposée pour le traitement des céphalées en grappe. La zone cible de la SCP a été sélectionnée grâce à des études morphométriques. Les premières interventions ont été réalisées par l'équipe de recherche italienne de Leone et al. en 2000. Cependant, en raison de résultats décevants à long terme et de risques importants, y compris des risques mortels (hémorragie intracérébrale létale induite par l'implantation), la SCP pour les céphalées en grappe est restée une thérapie expérimentale et a été largement abandonnée. La seule étude en double aveugle contrôlée par placebo réalisée à ce jour n'a pas mis en évidence de différence significative entre la stimulation réelle et la stimulation simulée (Fontaine et al., 2010). En règle générale, un traitement médicamenteux préventif est nécessaire malgré la SCP. La surveillance intensive à long terme, l'ajustement du traitement médicamenteux et l'évolution naturelle de la maladie sont autant de facteurs qui influencent les résultats du traitement. Une efficacité insuffisante du traitement est parfois attribuée à un positionnement incorrect des électrodes lors de la SCP.
Il n'est pas encore établi si les modifications structurelles de l'hypothalamus postérieur inférieur sont corrélées à la douleur, au sens d'une activation non spécifique, si elles résultent d'un traitement antérieur ou si elles sont la cause des céphalées. L'application de la stimulation cérébrale profonde pour les céphalées en grappe demeure expérimentale et nous n'envisageons aucune utilisation en pratique clinique. Les travaux de Leone et al. (2001) sont considérés comme le seul exemple d'application thérapeutique des résultats d'imagerie, mais leur efficacité n'a pas été démontrée. À notre avis, ces études ne justifient pas une utilisation clinique.
La stimulation de zones cibles et l'amélioration occasionnelle qui en découle ne doivent pas laisser supposer que ces régions jouent un rôle causal crucial dans la physiopathologie des céphalées en grappe. La stimulation de structures neurales, tant dans le système nerveux central que périphérique, peut moduler de nombreux mécanismes de la douleur et avoir un effet non spécifique sur le processus douloureux. Ceci est également corroboré par les taux d'amélioration des céphalées en grappe et d'autres syndromes douloureux suite à la stimulation du grand nerf occipital ou du ganglion sphénoïdal. À l'heure actuelle, il ne semble pas suffisamment justifié de tirer des conclusions sur la cause des céphalées en grappe à partir des seuls résultats de la stimulation. Le rôle hypothétique de l'hypothalamus postéro-inférieur dans les céphalées en grappe est illustré dans la figure ci-contre (abréviations : GCRP peptide lié au gène de la calcitonine ; SPG : ganglion sphénopalatin ; SSN : noyau salivaire supérieur ; VIP polypeptide intestinal vasoactif).
Des études récentes ont analysé l'évolution à long terme des céphalées en grappe et les modifications de la substance grise. Nägel et al. (2011) ont examiné 75 patients souffrant de céphalées en grappe (22 présentant des crises épisodiques en période active, 35 des crises épisodiques en dehors de la période active et 18 des céphalées en grappe chroniques) et comparé les modifications de la substance grise à celles de 61 sujets témoins sains appariés, à l'aide de la morphométrie basée sur les voxels (VBM). Les patients ayant présenté des crises aiguës récentes de céphalées en grappe en période active ont montré les réductions les plus marquées de la substance grise au sein du système central de traitement de la douleur. Chez les patients souffrant de céphalées en grappe chroniques, des modifications supplémentaires ont été détectées dans le cortex cingulaire antérieur, l'amygdale et le cortex somatosensoriel secondaire. En dehors de la période active, aucune modification n'a été observée dans ces régions chez les patients souffrant de céphalées en grappe épisodiques. Aucune modification de l'hypothalamus n'a été constatée, ni dans les sous-groupes, ni dans l'ensemble du groupe. Ces données démontrent une perte de substance grise dans les systèmes centraux de traitement de la douleur, en particulier chez les patients souffrant de céphalées en grappe chroniques. En revanche, aucune modification n'a été observée au niveau de l'hypothalamus. Ces résultats sont similaires à ceux obtenus chez des patients souffrant d'autres affections douloureuses. Ils confortent l'hypothèse selon laquelle les modifications morphologiques sont des conséquences de la douleur aiguë et non sa cause première. Ces modifications pourraient être corrélées aux processus de chronicisation. Cette hypothèse est étayée par les anomalies particulièrement marquées observées chez les patients atteints de céphalée en grappe chronique. Aucune modification n'ayant été détectée au niveau de l'hypothalamus, le rôle de cette structure dans le développement de la céphalée en grappe demeure controversé (Nägel et al., 2011 ; Holle et Obermann, 2011).
Inflammation du sinus caverneux
Les phlébographies orbitaires réalisées chez des patients souffrant de céphalées en grappe pendant les crises actives ont révélé des signes de processus inflammatoires d'origine indéterminée au niveau du sinus caverneux et de la veine ophtalmique supérieure. Dans le sinus caverneux, les fibres sensitives du nerf ophtalmique, les fibres sympathiques innervant la paupière, l'œil, le visage, l'orbite et les vaisseaux rétro-orbitaires ipsilatéraux, les vaisseaux veineux drainant l'orbite et le visage, ainsi que l'artère carotide interne sont regroupés dans un espace osseux très restreint (voir figure). Les processus inflammatoires locaux peuvent ainsi affecter à la fois les fibres nerveuses sensitives et autonomes, ainsi que les vaisseaux veineux et artériels. L'irritation des fibres nerveuses est envisageable, soit directement par des neuropeptides inflammatoires, soit par compression mécanique exercée par des vaisseaux enflammés et gonflés. Cette théorie peut expliquer la douleur de la céphalée en grappe et ses divers symptômes associés. La capacité des substances vasodilatatrices à provoquer des crises en grappe pendant les périodes actives de crises en grappe (alcool, nitroglycérine, histamine, hypoxie) et des substances vasoconstrictrices (oxygène, sumatriptan, ergotamine) à les terminer rapidement est également compatible avec le modèle.
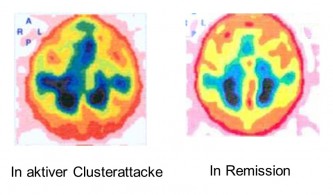
On suppose qu'une réponse inflammatoire basale est présente pendant les périodes actives de céphalées en grappe, et qu'elle s'exacerbe lors des crises. Les phlébographies orbitaires, suggérant un processus inflammatoire, ont été réalisées entre les crises, au cours d'une période active de céphalées en grappe. Chez les patients souffrant de céphalées en grappe chroniques ou épisodiques, une scintigraphie myocardique de perfusion (SPECT) à l'albumine marquée au Tc-99m a été effectuée 10 minutes, 1 heure, 3 heures et 6 heures après l'injection de 600 MBq d'albumine sérique humaine (HSA) marquée au Tc-99m, pendant une période active de céphalées en grappe. Dans le groupe témoin sain, une distribution hétérogène de l'activité a été observée. En revanche, chez les patients souffrant de céphalées en grappe, une accumulation du traceur a été constatée au niveau du sinus caverneux, du sinus sphéno-pariétal, de la veine ophtalmique, du sinus pétreux et du sinus sigmoïde pendant la phase active (voir figure). Le côté de la céphalée en grappe et la zone d'extravasation protéique correspondaient chez tous les patients. Après un traitement prophylactique efficace par vérapamil ou corticostéroïdes, l'augmentation de la fixation du traceur a disparu. Une crise de céphalée en grappe est ainsi associée à une extravasation régionale de protéines plasmatiques dans les sinus veineux de la base du cerveau, signe d'une inflammation vasculaire locale. Un traitement efficace par vérapamil ou corticostéroïdes bloque à la fois l'extravasation plasmatique ipsilatérale et les crises de céphalée en grappe. Dans la céphalée en grappe chronique, cette réaction inflammatoire sous-jacente est continue, tandis que dans la forme épisodique, elle est seulement périodique. Ceci explique également l'efficacité élevée et fiable des corticostéroïdes anti-inflammatoires dans la prophylaxie des céphalées en grappe. Le sinus caverneux est traversé par l'artère carotide, les nerfs optiques, les nerfs ophtalmiques et le nerf facial. Tous ces nerfs sont affectés lors d'une crise de céphalée en grappe. Cette théorie explique la douleur liée à la céphalée en grappe et ses divers symptômes associés. La capacité des substances vasodilatatrices à provoquer des crises de céphalée en grappe pendant les périodes actives (alcool, nitroglycérine, histamine, hypoxie) et celle des substances vasoconstrictrices (oxygène, sumatriptan, ergotamine) à les interrompre rapidement est également compatible avec ce modèle.
L'image ci-contre illustre la preuve diagnostique d'une extravasation plasmatique unilatérale, expression d'une vascularite du sinus caverneux chez un patient en phase active de poussées. Du côté des poussées, au niveau du sinus caverneux droit et du sinus pétreux supérieur, des signes nets d'inflammation sont observés sous forme de fuites plasmatiques asymétriques au niveau des veines, mises en évidence par scintigraphie SPECT à l'albumine marquée au Tc-99m, 10 minutes, 1 heure, 3 heures et 6 heures après l'injection de 600 MBq d'albumine sérique humaine (HSA) marquée au Tc-99m. Alors qu'une symétrie initiale du système vasculaire veineux est observée après 10 minutes, une asymétrie marquée apparaît après trois heures, due à l'augmentation progressive de l'extravasation plasmatique. Ces modifications ne sont pas observées pendant la phase de rémission
L'apparition de la douleur pendant le sommeil, la position assise ou le lever du patient, ainsi que son agitation motrice, s'expliquent : le drainage veineux du sinus caverneux est moins efficace en position couchée, en raison des conditions hydrostatiques, qu'en position assise ou debout. On peut donc supposer qu'une réaction inflammatoire sous-jacente est présente lors des périodes de crises actives, et qu'elle s'exacerbe lors des attaques. Ceci explique également pourquoi le tabagisme et les changements de saison, avec leur susceptibilité accrue aux sinusites, sont associés à une probabilité plus élevée de crises actives.
Les anti-inflammatoires, comme la cortisone, entraînent un arrêt rapide des crises de céphalée en grappe. Cependant, en raison de leurs effets secondaires à long terme, ils ne conviennent pas à un traitement prolongé. Les inhibiteurs calciques, comme le vérapamil, préviennent l'inflammation en empêchant l'extravasation plasmatique et sont adaptés à un traitement au long cours. Les anti-inflammatoires non stéroïdiens (AINS), comme l'indométacine, peuvent être particulièrement efficaces dans certaines formes de céphalée en grappe, comme l'hémicrânie paroxystique chronique, mais sont généralement insuffisants pour traiter l'ensemble des crises. Il en va de même pour l'aspirine, l'ibuprofène, etc. Ces médicaments sont inefficaces lors d'une crise aiguë, pourtant de nombreuses personnes les prennent et pensent, à tort, que la diminution des crises après 2 à 3 heures est due à ces médicaments. Des cas d'efficacité de la warfarine (Coumadin) lors des crises de céphalée en grappe ont également été rapportés ; ce médicament prévient probablement l'aggravation de l'agrégation plaquettaire dans le sinus caverneux causée par la vascularite veineuse. L'efficacité de l'azothioprine observée dans les cas rapportés pourrait reposer sur une réduction de la réponse inflammatoire sous-jacente.
Modifications neuronales
Diverses méthodes électrophysiologiques ont été utilisées pour analyser les modifications de l'activité neuronale au cours des crises de céphalées en grappe. Dans ce contexte également, l'analyse comparative directe et l'analyse de la période de crise par rapport à la période de rémission sont utiles. La mise en évidence d' une perturbation des voies sensorielles peut être obtenue grâce à l'étude des potentiels évoqués auditifs du tronc cérébral et des potentiels évoqués somesthésiques.
Les réactions pupillaires chez les patients souffrant de céphalée en grappe ont été analysées en détail Le myosis est l'une des caractéristiques les plus marquantes de cette affection. Le réflexe photomoteur consensuel observé plus rapidement et plus prononcé chez ces patients dérèglement du côté atteint qu'en phase de rémission. La réponse pupillaire à la stimulation électrique douloureuse du nerf sural diminuée du côté affecté par la céphalée en grappe . Cette diminution de la dilatation pupillaire pourrait être due à une augmentation de la libération de neuropeptides tels que la substance P et la neurokinine A, induisant une constriction pupillaire directe. La stimulation électrique directe du nerf infratrochléaire provoque également une constriction pupillaire unilatérale , non médiée par des mécanismes cholinergiques. Cette réaction peut également être induite par la libération de substance P et de neurokinine A. Ces neuropeptides peuvent être libérés en plus grande quantité lors des crises de céphalées en grappe (voir ci-dessus), car la réponse à la stimulation du nerf infratrochléaire significativement plus faible . Ces observations suggèrent que non seulement les voies sympathiques, mais aussi les fibres sensitives du nerf trijumeau pourraient jouer un rôle important dans la physiopathologie des céphalées en grappe. Un autre argument en faveur d'une altération des propriétés sensorielles est l'hypersensibilité à la douleur observée chez les patients souffrant de céphalées en grappe pendant les périodes intercritiques, particulièrement marquée du côté affecté par la céphalée. Pendant la rémission, la sensibilité à la douleur revient à la normale. Conjuguées à l'augmentation de la réponse à la stimulation du nerf infratrochléaire, ces observations peuvent être interprétées signe d'excitabilité accrue des neurones nociceptifs du nerf trijumeau
D'autres modifications de la réponse pupillaire sont également observées lors de la stimulation pharmacologique , l'instillation bilatérale de sympathomimétiques indirects tels que l'hydroxyamphétamine entraîne une mydriase réduite du côté atteint pendant la phase active, en dehors des crises. Inversement, l'administration d'un sympathomimétique direct tel que la phényléphrine dans l'œil atteint de céphalée en grappe provoque une mydriase accrue . Ces observations suggèrent une diminution de l'activité sympathique du côté symptomatique . La sudation induite expérimentalement, par exemple par application de chaleur, est également réduite du côté symptomatique chez les patients atteints pendant la phase active, en dehors des crises. En revanche, l'administration de pilocarpine entraîne une augmentation de la sudation du côté symptomatique. Ces observations peuvent également être interprétées comme la preuve d' un dysfonctionnement des fibres sympathiques hypersensibilité des récepteurs postsynaptiques. Cependant, la localisation de l'hyperfonction sympathique n'est pas nécessairement périphérique , car des observations similaires peuvent également être faites dans le syndrome de Horner central